
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

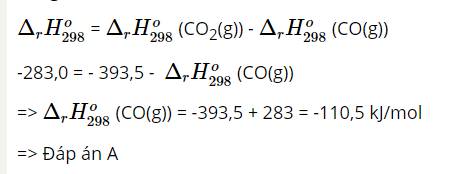

\(C_2H_6+\dfrac{7}{2}O_2->2CO_2+3H_2O\\ \Delta_rH^o_{298}=2\left(-393,5\right)+3\left(-285,8\right)-\left(-84,7\right)\\ \Delta_rH^o_{298}=-1559,7kJ\)
Phương trình nhiệt hoá học thì không cần ghi điều kiện nhé.

\(\Delta_rH^o_{298}=2\left(-825,5\right)+8\left(-296,8\right)-4\left(-177,9\right)\\ \Delta_rH^o_{298}=-3313,8\left(kJ\right)\)

\(N_2O_4+3CO->N_2O+3CO_2\\ \Delta_rH^o_{298}=82,05+3\left(-393,50\right)-\left(9,16+3\left(-110,50\right)\right)\\ \Delta_rH^o_{298}=-776,11kJ\)

\(\Delta_fH^{^{ }o}_{298}\left[CH_4\right]=-\left(-890,3-\left(-393,5\right)-\left(-285,8\right)\right)\\ \Delta_fH^{^{ }o}_{298}\left[CH_4\right]=211kJ\cdot mol^{-1}\)

\(\Delta_rH^o_{298}=\left(612+4\cdot418\right)+436-\left(346+6\cdot418\right)\\ \Delta_rH^o_{298}=-134kJ\cdot mol^{-1}\)
Ethylene có 4 C-H, năng lượng của nó đâu?
Không nên dùng AI để tính toán. Chưa chắc là nó sẽ luôn cho ra kết quả đúng đâu mà dùng vô tội vạ như vậy.

\(\Delta_rH^o_{298}=436+243-2\cdot432\\ \Delta_rH^o_{298}=-185kJ\cdot mol^{-1}\)
Để tính biến thiên enthalpy chuẩn của phản ứng, ta có thể sử dụng công thức sau:
ΔH° = (tổng năng lượng liên kết sản phẩm) - (tổng năng lượng liên kết phản ứng chất). Trong trường hợp này, ta có: Tổng năng lượng liên kết phản ứng chất = Eb(H-H) + Eb(Cl-Cl) = 436 + 243 = 679 kJ/mol Tổng năng lượng liên kết sản phẩm = 2Eb(H-Cl) = 2 * 432 = 864 kJ/mol Vậy biến thiên enthalpy chuẩn của phản ứng là: ΔH° = 864 - 679 = 185 kJ/mol.

\(\Delta_rH^{^o}_{298}=945+494-2\cdot607=+225kJ\\ \Rightarrow D\)
Bạn ơi, bạn có biết gì về Eb không vậy? Mình tính Eb(cđ) - Eb(sp) mà? Công thức đó đâu ra vậy?

nC2H2 = 1/26 (mol)
Đốt cháy 1/26 mol C2H2 tỏa ra 49,98 kJ
=> Đốt cháy 1 mol C2H2 tỏa ra x kJ
=> x = 1 x 49,98 : (1/26) = 1299,48 kJ
=> ${\Delta _r}H_{298}^0$ = -1299,48 kJ (vì đây là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm)