Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

– Phần 2: naxit = nkhí thoát ra = 0,2 mol
→ Giả sử Z là CH3OH
→ Axit là HCOOH → nAg tạo ra > 0,2.2 = 0,4 → Loại
Z có dạng RCH2OH (R khác H) → nRCHO = nAg : 2 = 0,2 mol
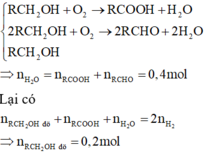
Rắn khan gồm: 0,2 mol RCH2ONa; 0,2 mol RCOONa; 0,4 mol NaOH.
→ 0,2.(MR + 53) + 0,2.(MR + 67) + 0,4. 40 = 51,6 g.
→ MR = 29 → Z là C3H7OH với số mol: 0,6.3 = 1,8 mol = nKOH đã phản ứng
→ KOH dư 0,6 mol
→ 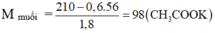
→ Este X là CH3COOC3H7 → X là propyl axetat
→ Đáp án B

Chọn đáp án B.
Giải phần 2: ![]()
Nếu R là H, tức axit là HCOOH thì 0,2 mol sẽ tham gia phản ứng tráng bạc tạo 0,4 mol Ag.
Điều này có nghĩa là trong T chỉ chứa axit và ancol dư, không có anđehit → không hợp lý.!
R khác H thì + A g N O 3 / N H 3 chỉ có thể là anđehit RCHO sinh A g k t → n R C H O = 0 , 2 mol.
Phản ứng oxi hóa không hoàn toàn: 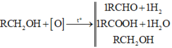
Giải phần 3: R C H 2 O H + N a → A C H 2 O N a + 1 / 2 H 2 ( k h i )
![]()
Tổng số mol H2 thu được là 0,4 mol, axit có 0,2 mol, nước là 0,4 mol → n a n c o l = 0 , 2 mol.
Khối lượng chất rắn: 51,6= 0,2.(R+53)+0,2.(R+67)+0,4.40=> R=29 là gốc C 2 H 5 .
« Giải bài tập thủy phân 1,8 mol X + 2,4 mol KOH
→ 210 gam (R'COOK+KOH dư)+0,18 mol ancol.
(chú ý nhân 3 kết quả tính toán trên) Ta có: 210= 1,8(R' +83)+0,6.56 => R'= 15 là gốc C H 3 .
Vậy, este X là C H 3 C O O C H 2 C H 2 C H 3 → tên gọi: propyl axetat.

Đáp án B
· Phần 1: + NaOH ® 0,045 mol H2
Þ Chứng tỏ oxit sắt phản ứng hết, Al dư:
![]()
Chất rắn còn lại là Fe:
![]()
· Phần 1: Có
Þ Chứng tỏ phần 2 nhiều gấp 3 lần phần 1.
· Khối lượng kết tủa lớn nhất khi toàn bộ lượng Al3+ và Fe3+ tạo kết tủa
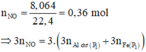
Þ Chứng tỏ phần 2 nhiều gấp 3 lần phần 1.
· Khối lượng kết tủa lớn nhất khi toàn bộ lượng Al3+ và Fe3+ tạo kết tủa.
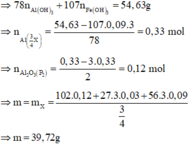

Đáp án A
Ta có khối lượng mỗi phần là 30,66 gam.
Cho phần một tác dụng với NaOH dư thu được 0,09 mol H2 do vậy trong X chứa Al dư.
Vậy trong mỗi phần chứa Fe, Al2O3 và Al dư 0,06 mol.
Cho phần 2 tác dụng với 1,74 mol HNO3 thu được 0,18 mol NO. Cô cạn dung dịch Y thu được các muối, nung rắn tới khối lượng không đổi thu được rắn chứa Al2O3 và Fe2O3 có số mol bằng nhau.
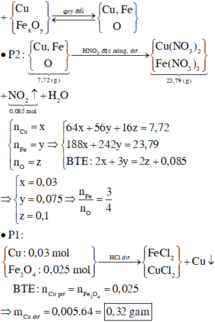
Gọi số mol của Fe, Al2O3 trong mỗi phần lần lượt là a, b
![]()
Và a=2b+0,06
Giải hệ: a=0,3; b=0,12.
Gọi x là số mol NH4NO3 có thể tạo ra.
Bảo toàn N:
n N O 3 - t r o n g m u o i K l = 1 , 74 - 0 , 18 - 2 x = 1 , 56 - 2 x
Bảo toàn e: 1 , 56 - 2 x = 0 , 12 . 6 + 0 , 18 . 3 + 8 x
Vậy NO3– trong muối là 1,5 mol.
Muối trong Y gồm Al(NO3)3 0,3 mol, Fe(NO3)2 0,3 mol và NH4NO3 0,03 mol.
Cho Y tác dụng với Na2CO3 dư thu được kết tủa là Al(OH)3 0,3 mol và FeCO3 0,3 mol.
→ a = 58 , 2 g

Đáp án B
Chất rắn m1 là Cu. Bảo toàn e có 2nCu=3nNO
→ 2b = 2V/70
Gọi số mol: Mg là x; Cu là y; Al là z và NH4NO3 là t
Ta có hệ phương trình
(1) 2x +3y = 2n(H2) = 0,88
(2) 24x + 64y + 27z = 19,92
(3) 148x + 188y + 213z + 80t = 97,95
(4) 2x + 2y + 3t = 3n(NO) + 8n(NH4NO3) = 3V/22,4 + 8t = 6,25y + 8t
→ x = 0,08; y = 0,18; z = 0,24
→ %Mg = 9,64%

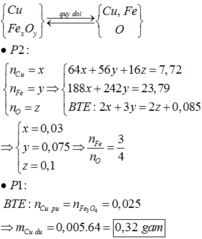

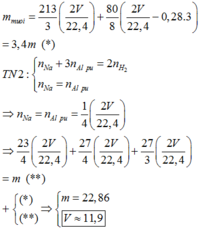
Đáp án C
Vì khối lượng hai phần bằng nhau nên thể tích khí H2 thu được ở hai trường hợp bằng nhau.
Khối lượng mỗi phần là 11,6 gam.