Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Quy hỗn hợp X thành Fe phản ứng (a mol) và O (b mol) và 1,46 g Fe không tan
Bảo toàn khối lượng => 56a + 16b + 1,46 = 18,5

Đáp án B

Đáp án A
Do Fe dư nên chỉ tạo ra Fe2+.
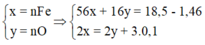
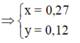
4H+ + NO3- + 3e → NO + 2H2O
2H+ + O + 2e → H2O
=> nHNO3 = nH+ = 4nNO + 2nO = 4.0,1 + 2.0,12 = 0,64
=> [HNO3] = 0,64/0,2 = 3,2M => Chọn A.

vì trong hỗn hợp còn kim loại Fe dư nên muối là Fe(NO3)2
quy đổi hỗn hợp ban đầu về hỗn hợp có x mol Fe và y mol O
(x mol Fe này là lượng Fe phản ứng không tính lượng dư, sau phản ứng klượng Fe này tạo hết thành muối nên nFe(NO3)2 = nFe = x)
⇒ 56x + 16y = 18,5 - 1,46 (1)
nNO = 2,24/22,4 =0,1
áp dụng định luật bảo toàn e
Fe → Fe+2 + 2e O +2e → O-2
x → 2x y → 2y
N+5 + 3e → N+2
0,3← 0,1
tổng số mol e nhường = tổng số mol e nhân
⇒ 2x = 2y + 0,3 (2)
từ (1) và (2) ta có
x= 0,27 ⇒nFe =0,27 ⇒ nFe(NO3)2 = 0,27 ⇒mFe(NO3)2 = 48,6 g

Đáp án B
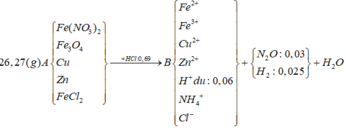
Tính nhanh được nN2O = 0,03 mol và nH2 = 0,025 mol; nFe = 0,09 mol
Do khi cho dung dịch AgNO3 dư vào B thấy có khí NO thoát ra nên B có chứa HCl dư
nHCl dư = nH+ dư = 4nNO = 0,06 mol (do 3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O)
=> nHCl pu với A = 0,69 – 0,06 = 0,63 mol
Ta có: A + HCl → muối + khí + H2O
BTKL => mH2O = mA + mHCl pư với A – m muối – m khí = 26,27 + 0,63.36,5 – 0,03.44 – 0,025.2 = 4,5 (g)
=> nH2O = 0,25 mol
BT “H”: nNH4+ = (nHCl – nH+ dư - 2nH2 – 2nH2O):4 = (0,69-0,06-2.0,025-2.0,25):4 = 0,02 mol
BT “N”: nFe(NO3)2 = (2nN2O + nNH4+):2 = (2.0,03 + 0,02):2 = 0,04 mol
BT “O”: 6nFe(NO3)2 + 4nFe3O4 = nN2O + nH2O => 6.0,04+4nFe3O4 = 0,03+0,25 => nFe3O4 = 0,01 mol
BT “Fe”: nFe = nFe(NO3)2 + 3nFe3O4 + nFeCl2 => 0,09 = 0,04 + 3.0,01 + nFeCl2 => nFeCl2 = 0,02 mol
Khi cho B + AgNO3 dư:


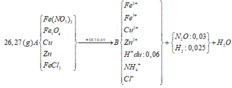
Tính nhanh được nN2O = 0,03 mol và nH2 = 0,025 mol; nFe = 0,09 mol
Do khi cho dung dịch AgNO3 dư vào B thấy có khí NO thoát ra nên B có chứa HCl dư
nHCl dư = nH+ dư = 4nNO = 0,06 mol (do 3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O)
=> nHCl pu với A = 0,69 – 0,06 = 0,63 mol
Ta có: A + HCl → muối + khí + H2O
BTKL => mH2O = mA + mHCl pư với A – m muối – m khí = 26,27 + 0,63.36,5 – 0,03.44 – 0,025.2 = 4,5 (g)
=> nH2O = 0,25 mol
BT “H”: nNH4+ = (nHCl – nH+ dư - 2nH2 – 2nH2O):4 = (0,69-0,06-2.0,025-2.0,25):4 = 0,02 mol
BT “N”: nFe(NO3)2 = (2nN2O + nNH4+):2 = (2.0,03 + 0,02):2 = 0,04 mol
BT “O”: 6nFe(NO3)2 + 4nFe3O4 = nN2O + nH2O => 6.0,04+4nFe3O4 = 0,03+0,25 => nFe3O4 = 0,01 mol
BT “Fe”: nFe = nFe(NO3)2 + 3nFe3O4 + nFeCl2 => 0,09 = 0,04 + 3.0,01 + nFeCl2 => nFeCl2 = 0,02 mol
Khi cho B + AgNO3 dư:
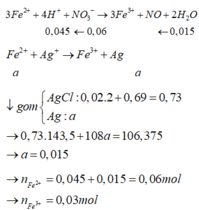

Đáp án B
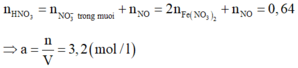

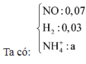
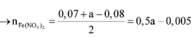
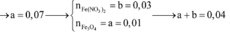
Đáp án B
Vì sau phản ứng còn dư kim loại nên trong dung dịch B tồn tại Fe(NO3)2. Các phản láng xảy ra:
Như vậy trong toàn bộ các quá trình, số oxi hóa của sắt trong Fe và Fe3O4 đều về số oxi hóa +2.
Theo định luật bảo toàn mol electron, ta có: