Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

này cái thằng kia muốn gây sự hả mà tự nhiên đi quá người ta

Fe+2HCl--->FeCl2+H2
H2+CuO-->Cu+Fe
Ta có
n Fe=2,24/56=0,04(mol)
Theo pthh1
n H2=n Fe=0,04(mol)
n CuO=4,2/80=0,0525(mol)
--->CuO dư
n CuO dư=0,0525-0,04=0,0125(mol)
m CuO=0,0125.80=1(g)
n Cu=n H2=0,04(mol)
m Cu=0,04.64=2,56(g)
m chất rắn =1+2,56=3,56(g)

a)
\(n_{Fe}=\frac{2,24}{56}=0,04\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,04 ________________ 0,04
\(V_{H2}=0,04.22,4=0,896\left(l\right)\)
b)
\(n_{CuO}=\frac{4,2}{80}=0,0525\left(mol\right)\)
\(PTHH:CuO+H_2\rightarrow Cu+H_2O\)
TPU____0,0525__0,04________
PU____0,04____ 0,04___0,04______
SPu ___0,0125___ 0 ___ 0,04________
\(\rightarrow m_{Cr}=0,0125.80+0,04.64=3,56\left(g\right)\)
a, PTHH ( I ) : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{Fe}=\frac{m_{Fe}}{M_{Fe}}=\frac{2,24}{56}=0,04\left(mol\right)\)
- Theo PTHH : \(n_{H_2}=n_{Fe}=0,04\left(mol\right)\)
-> \(V_{H_2}=n_{H_2}.22,4=0,04.22,4=0,896\left(l\right)\)
b, \(n_{CuO}=\frac{m_{CuO}}{M_{CuO}}=\frac{4,2}{64+16}=0,0525\left(g\right)\)
PTHH ( II ) :........ \(CuO+H_2\rightarrow Cu+H_2O\)
Trước phản ứng :.0,0525....0,04.........
Trong phản ứng :..0,04.......0,04....
Sau phản ứng : ....0,0125.....0.........
-> Sau phản ứng H2 phản ứng hết, CuO còn dư ( dư 0,0125 mol )
- Theo PTHH ( II ) : \(n_{Cu}=n_{H_2}=0,04\left(mol\right)\)
-> \(m_{CuO}=n_{CuO}.M_{CuO}=0,04.64=2,56\left(g\right)\)
\(m_{CuO}=n_{CuO}.M_{CuO}=0,0125.\left(64+16\right)=1\left(g\right)\)
- Ta có : mchất rắn sau = mCuO dư + mCu = 1 + 2,56 = 3,56 ( g )

mCuO giảm= mO
H2+ O -> H2O
=> nH2= nO= 0,35 mol
=> nCl= nHCl= 2nH2= 0,7 mol
m= m kim loại+ mCl= 14,8+ 0,7.35,5= 39,65g
mCuO giảm= mO
H2+ O -> H2O
=> nH2= nO= 0,35 mol
=> nCl= nHCl= 2nH2= 0,7 mol
m= m kim loại+ mCl= 14,8+ 0,7.35,5= 39,65g

\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
Do khi hòa tan A vào HCl thu được hỗn hợp khí
=> Trong A chứa H2, H2S
=> Al dư, S hết
PTHH: 2Al + 3S --to--> Al2S3
0,2<--0,3------>0,1
2Al + 6HCl --> 2AlCl3 + 3H2
0,1----------------------->0,15
Al2S3 + 6HCl --> 2AlCl3 + 3H2S
0,1------------------------>0,3
=> \(\overline{M}_X=\dfrac{0,15.2+0,3.34}{0,15+0,3}=\dfrac{70}{3}\left(g/mol\right)\)
=> \(d_{X/H_2}=\dfrac{\dfrac{70}{3}}{2}=\dfrac{35}{3}\)

Đáp án B
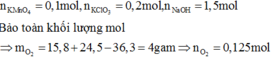
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()
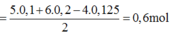


Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.
Fe + 2HCl → Fe Cl 2 + H 2 (1)
Theo PTHH (1) ta có
n H 2 = n Fe = 2,24/56 = 0,04 mol
CuO + H 2 → Cu + H 2 O (2)
Theo PTHH (2) :
Số mol CuO phản ứng : n CuO = n H 2 = 0,04 mol.
Số mol Cu tạo ra là 0,04 mol.
Số mol CuO dư 4,2/80 - 0,04 = 0,0125 mol
Sau phản ứng trong ống nghiệm có: m Cu = 64 x 0,04 = 2,56g
m CuO = 80 x 0,0125 = 1g
Khối lượng chất rắn : 1+ 2,56=3,56 (g).