Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài làm:
nH2= 1,344 / 22,4=0,06 mol
Khối lượng Fe và Al là: 2,52 ‐ 0,3= 2,22 g
Fe + 2HCl ‐‐> FeCl2 + H2
x mol 2xmol x mol
2Al + 6HCl ‐‐> 2AlCl3 + 3H2
y mol 3ymol 3/2 mol
56x + 27y = 2,22 ﴾1﴿
x + 3/2y = 0,06 ﴾2﴿
Từ﴾1﴿ và ﴾2﴿ ta có => x= 0,03
=> y=0,02
a/ mFe=0,03.56=1,68g
mAl=0,02.27=0,54g
%mCu=﴾0,3/2,52﴿.100=11,9%
%mFe=﴾1,68/2,52﴿.100=66,6%
%mAl=21,5%
b/ m\(_{ct}\) =0,12.36,5=4,38g
%C \(_{hcl}\)= ﴾4,38/200﴿.100=2,19%

PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Theo PTHH: \(n_{Mg}=n_{H_2}=0,6\left(mol\right)\)
=> \(m_{Mg}=0,6.24=14,4\left(g\right)\)
=> \(m_{Cu}=50-14,4=35,6\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%Mg=\dfrac{14,4}{50}.100=28,8\%\\\%Cu=\dfrac{35,6}{50}.100=71,2\%\end{matrix}\right.\)
\(n\)H2 =\(\dfrac{13,44}{22,4}\) =0,6(mol)
PTHH:
Mg +HCl →MgCl2 + H2
0,6 mol ←0,6 mol
a) \(m\)Mg =0,6. 24 =14,4(g)
\(m\)Cu= 50- 14,4= 35,6(g)
b)\(m\)%Mg= \(\dfrac{14,4}{50}\).100%= 28,8%
\(m\)%Cu=100%- 28,8%= 71,2%

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,1<-------------------------0,15
=> \(\%m_{Al}=\dfrac{0,1.27}{9,1}.100\%=29,67\%=>\%m_{Cu}=100\%-29,67\%=70,33\%\)

Phần 1 :
$m_{Cu} = 0,4(gam)$
Gọi $n_{Fe} = a ; n_{Al} = b \Rightarrow 56a + 27b + 0,4 = 1,5 : 2 = 0,75(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$n_{H_2} = a + 1,5b = \dfrac{896}{1000.22,4} = 0,04(2)$
Từ (1)(2) suy ra a = -0,025 < 0$
$\to$ Sai đề

a, Cu không tác dụng với dd HCl.
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,2.65=13\left(g\right)\)
\(\Rightarrow m_{Cu}=19,4-13=6,4\left(g\right)\)
c, Ta có: \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{13}{19,4}.100\%\approx67,01\%\\\%m_{Cu}\approx32,99\%\end{matrix}\right.\)
Bạn tham khảo nhé!

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,2\left(mol\right)\Rightarrow m_{Zn}=0,2.65=13\left(g\right)\)
\(\Rightarrow m_{Ag}=20-13=7\left(g\right)\)
b, \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{13}{20}.100\%=65\%\\\%m_{Ag}=100-65=35\%\end{matrix}\right.\)

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{Zn}=n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,2.65=13\left(g\right)\)
Bạn xem lại xem đề cho bao nhiêu gam hỗn hợp nhé, vì mZn đã bằng 13 (g) rồi.

\(a) m_{Cu} = 9,6(gam)\\ n_{Al} = a(mol) ; n_{Fe} = b(mol)\\ \Rightarrow 27a + 56b = 16,55 -9,6 =6,95(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{3,92}{22,4} = 0,175(2)\\ (1)(2) \Rightarrow a = 0,05 ; b = 0,1\\ m_{Al} = 0,05.27 = 1,35(gam); n_{Fe} = 0,1.56 = 5,6(gam)\)
\(b) n_{HCl} = 2n_{H_2} = 0,175.2 = 0,35(mol) \Rightarrow m_{HCl} = 0,35.36,5 = 12,775(gam)\)
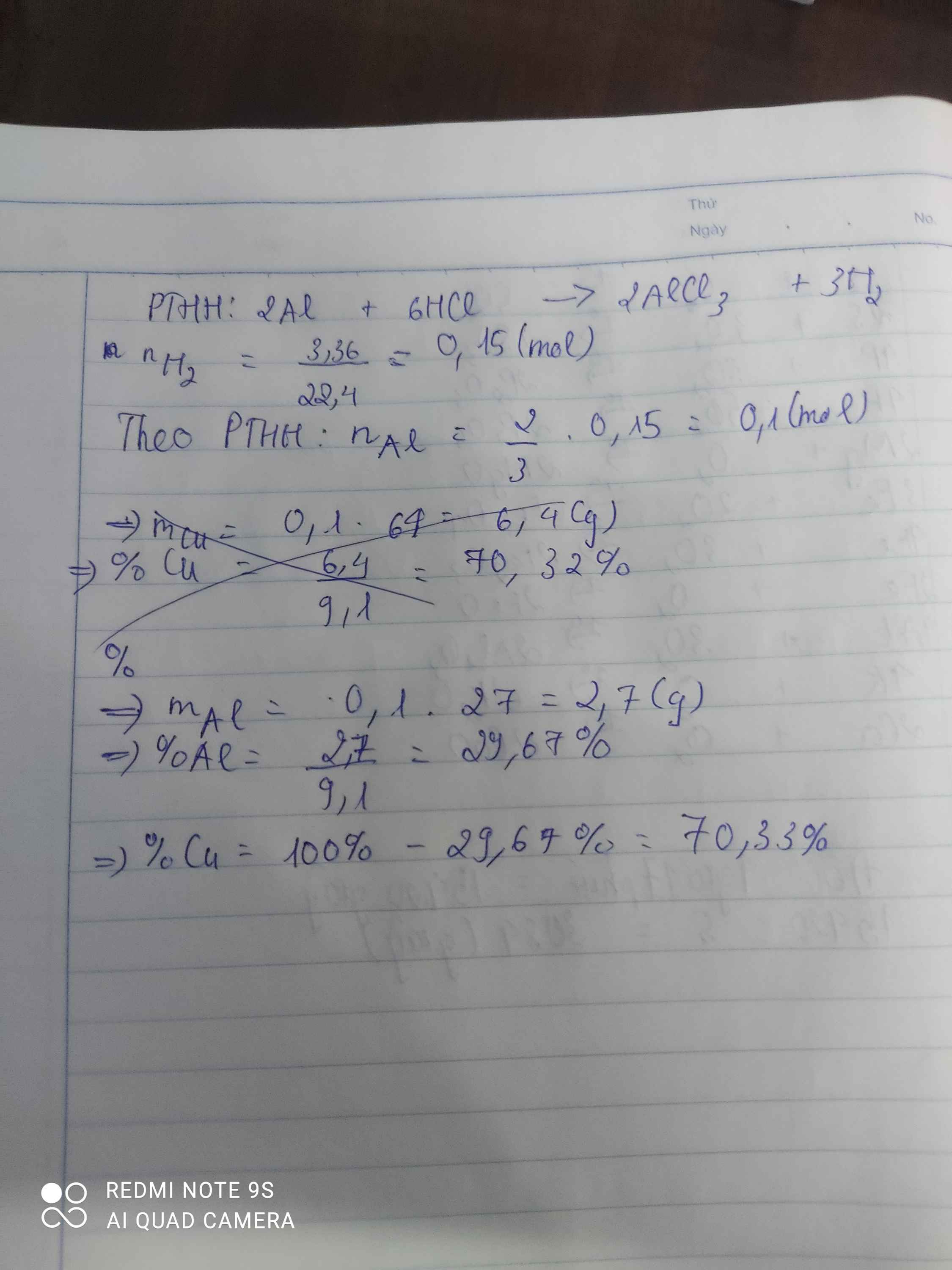
nH2= 1,344 / 22,4=0,06 mol
Khoi luong Fe va Al la 2,52 - 0,3= 2,22 g
Fe + 2HCl --> FeCl2 + H2
x mol 2xmol x mol
2Al + 6HCl --> 2AlCl3 + 3H2
y mol 3ymol 3/2 mol
56x + 27y = 2,22 (1)
x + 3/2y = 0,06 (2)
Tu (1) va (2) ta duoc => x= 0,03
=> y=0,02
a/ mFe=0,03.56=1,68g
mAl=0,02.27=0,54g
%mCu=(0,3/2,52).100=11,9%
%mFe=(1,68/2,52).100=66,6%
%mAl=21,5%
b/ mct=0,12.36,5=4,38g
%CHCl= (4,38/200).100=2,19%