Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.\\ m+m_{\left[O\right]}=16,2\\ n_{Cl^-}=2\dfrac{m_{\left[O\right]}}{16}\\ m+35,5\dfrac{m_{\left[O\right]}}{16}\cdot2=38,2\\ m=9,8;m_{\left[O\right]}=6,4\\ b.\\ V_{dd.acid}=v\left(L\right)\\ n_{H^+}=v+v=2v\left(mol\right)\\ n_{\left[O\right]}=\dfrac{6,4}{16}=0,4=\dfrac{2v}{2}\\ v=0,4\\ a=9,8+0,4\cdot35,5+0,4\cdot96=62,4g\)
`a)`
Bảo toàn KL:
`m_Y+m_{HCl}=m_{\text{muối}}+m_{H_2O}`
`->36,5n_{HCl}-18n_{H_2O}=38,2-16,2=22`
Mà bảo toàn H: `n_{HCl}=2n_{H_2O}`
`->n_{HCl}=0,8(mol);n_{H_2O}=0,4(mol)`
Bảo toàn O: `n_{O(Y)}=n_{H_2O}=0,4(mol)`
`->n_{O_2}=0,5n_{O(Y)}=0,2(mol)`
Bảo toàn KL: `m_X+m_{O_2}=m_Y`
`->m=16,2-0,2.32=9,8(g)`
`b)`
Đặt `V_{dd\ ax it}=x(l)`
`->n_{HCl}=x(mol);n_{H_2SO_4}=0,5x(mol)`
`n_{O(Y)}=0,4(mol)`
Bảo toàn electron: `n_{O(Y)}=1/2n_{H(ax it)}`
`->0,4=1/2(x+0,5x.2)`
`->x=0,4(l)`
`->n_{HCl}=0,4(mol);n_{H_2SO_4}=0,2(mol)`
Bảo toàn O: `n_{H_2O}=n_{O(Y)}=0,4(mol)`
Bảo toàn KL:
`m_Y+m_{HCl}+m_{H_2SO_4}=m_{\text{muối}}+m_{H_2O}`
`->a=16,2+0,4.36,5+0,2.98-0,4.18=43,2(g)`

a.Ta có n HCl = 1 . 0,25 = 0,25 mol
nH2SO4 = 0,5.0.25 = 0,125 mol
==> nH(X) = 0,25 + 0,125.2 = 0,5 mol
nH2 = 4,368/22,4 = 0,195 mol <=> nH= 0,195. 2 = 0,39 mol < 0,5 mol
Vậy sau phản ứng dung dịch B vẫn còn axit dư
b. Gọi số mol của Al và Mg lần lượt là x và y mol
Ta có phương trình 27x + 24y =3,87 (1)
Áp dụng định luật bảo toàn eletron ==> 3x + 2y = 0,195.2 (2)
Từ (1) , (2) ==> \(\left\{{}\begin{matrix}x=0,09\\y=0,06\end{matrix}\right.\)
mAl = 0,09 .27 = 2,43 gam , %mAl trong A = \(\dfrac{2,43}{3,87}\).100=62,8%
==> %mMg trong A = 100 - 62,8 = 37,2%

Bắt đầu xuất hiện kết tủa nghĩa là: NaOH đầu tiên sẽ trung hòa HCl dư trước
NaOH + HCldư → NaCl + H2O
0,2 ←0,2
→ 2V1 = 0,2 → V1 = 0,1
Đến khi kết tủa không thay đổi khối lượng thì khi đó kết tủa bị hòa tan hết.
3NaOH + AlCl3 → 3NaCl + Al(OH)3↓
3x ←x → x
NaOH + Al(OH)3 → NaAlO2 + 2H2O
x ←x
→ 0,2 + 4x = 0,6.2 → x = 0,25
=> y = 0,025
=> m = 17,75g

1.
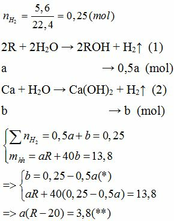
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
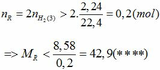
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
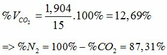
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
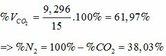

1)
$MgO + 2HCl to MgCl_2 + H_2O$
$Mg + 2HCl \to MgCl_2 + H_2$
2)
$n_{Mg} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$m_{Mg} = 0,1.24 = 2,4(gam)$
$m_{MgO} = 4,4 - 2,4 = 2(gam)$
3)
$n_{HCl} = 2n_{Mg} + 2n_{MgO} = 0,1.2 + \dfrac{2}{40}.2 = 0,3(mol)$
$V_{dd\ HCl} = \dfrac{0,3}{2} = 0,15(lít) = 150(ml)$

a) MgO + 2HCl ---> MgCl2 + H2O (1)
MgCO3 + 2HCl ---> MgCl2 + H2O + CO2 (2)
b) \(n_{CO_2}=\dfrac{m}{M}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> \(m_{MgCO_3}=n.M=0,1.84=8,4\left(g\right)\)
\(m_{MgO}=16-8,4=8\left(g\right)\)
c) \(n_{MgO}=\dfrac{m}{M}=\dfrac{8}{40}=0,2\left(mol\right)\)
=> \(n_{HCl\left(1\right)}=0,4\left(mol\right)\); nHCl(2) = 0,2(mol)
=> nHCl = 0.4 + 0,2 = 0,6 (mol)
=> VHCl = \(\dfrac{n}{C_M}=\dfrac{0,6}{1,5}=0,4\left(l\right)=400\left(ml\right)\)

– Gọi số mol các chất trong 15,15 gam hỗn hợp E lần lượt là a, b, c, d.
– Các phản ứng xảy ra:
Ca + 2H2O →Ca(OH)2 + H2
CaC2 + 2H2O →Ca(OH)2 + C2H2
Al4C3 + 12H2O →4Al(OH)3 + 3CH4
Ca(OH)2 + 2Al + 2H2O →Ca(AlO2)2 + 3H2
Ca(OH)2 + 2Al(OH)3 →Ca(AlO2)2 + 4H2O
– Áp dụng BTNT hidro: 2nH2O(đốt cháy) = 2nH2 + 2nC2H2 + 4nCH4
2b + 12c + 2d + 3a = 0,525.2 = 1,05
2(b + d) + 3(4c + a) = 1,05 = 2nCa + 3nAl
– Xét hỗn hợp X gồm: Al, Ca, C mX = mCa + mAl + mC = 15,15 (g)
mCa + mAl = 12,75 (g) nCa = 0,15 (mol) ; nAl = 0,25 (mol)
– Sản phẩm không có kết tủa nên dung dịch gồm: Ca(AlO2)2 và Ca(OH)2
– Bảo toàn nguyên tố Ca và Al dung dịch Y có 0,125 (mol) Ca(AlO2)2 ;
0,15 – 0,125 = 0,025 (mol) Ca(OH)2 và 0,4 (mol) HCl
Ca(OH)2 + 2HCl →CaCl2 + 2H2O
Ca(AlO2)2 + 2HCl + 2H2O →2Al(OH)3 + CaCl2
3HCl + Al(OH)3 →AlCl3 + 3H2O
– Áp dụng công thức tính nhanh: nHCl = 2nCa(OH)2 + 8nCa(AlO2)2 – 3n
0,4 = 0,025.2 + 8.0,125 – 3n
m1= 78.(0,65 : 3) = 16,9 (g)

a/ Số mol HCl = 0,35 x 2 = 0,7 mol
Giả sử hỗn hợp chỉ có Ca(HCO3)2
=> nCa(HCO3)2 = 59,13 / 162 = 0,365 mol
PTHH: Ca(HCO3)2 + 2HCl ===> CaCl2 + 2CO2 + 2H2O
0,35.........0,7..............................................0,7
Vì nX = \(\frac{59,13}{\overline{M}}>0,365>0,35\)
=> Chắc chắn hỗn hợp muối X còn dư
b/ Vì HCl phản ứng hết nên số mol CO2 tính theo HCl
Theo PTHH: nCO2 = 0,7 mol
=> VCO2(đktc) = 0,7 x 22,4 = 15,68 lít