Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Zn+2HCl->Zncl2+H2
0,1-------------------0,1
n Zn=0,1 mol
=>VH2=0,1.22,4=2,24l
=>C

$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$n_{KClO_3} = \dfrac{24,5}{122,5} = 0,2(mol)$
$n_{O_2} = \dfrac{3}{2}n_{KClO_3} = 0,3(mol)$
$V_{O_2} = 0,3.22,4 = 6,72(lít)
Đáp án B
\(KClO_3-^{t^o}\rightarrow KCl+\dfrac{3}{2}O_2\)
\(n_{O_2}=\dfrac{3}{2}n_{KClO_3}=\dfrac{3}{2}.\dfrac{24,5}{122,5}=0,3\left(mol\right)\)
=> \(V_{O_2}=0,3.22,4=6,72\left(l\right)\)
=> Chọn B

\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2....................0.2..........0.2\)
\(m_{ZnCl_2}=0.2\cdot136=27.2\left(g\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)

TTĐ:
\(m_{Zn}=6,5\left(g\right)\)
_______________
\(V_{H_2}=?\left(l\right)\)
\(m_{HCl}=?\left(g\right)\)
Giải
Số mol của 6,5 gam Zn:
\(n_{Zn}=\dfrac{m}{M}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Tỉ lệ: 1 : 2 : 1 : 1
Số mol: 0,1-> 0,2 : 0,2 : 0,2(mol)
a/ thể tích khí hiđro thu được:
\(V_{H_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
b/ Khối lượng của 0,2 mol HCl:
\(m_{HCl}=n.M=0,2.36,5=7,3\left(g\right)\)

a) \(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\)
b) \(n_{H_2}=n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ V_{H_2\left(ĐKTC\right)}=0,1.22,4=2,24\left(l\right)\)
c) \(n_{HCl}=2n_{Zn}=2.0,1=0,2\left(mol\right)\\ C_{M_{ddHCl}}=\dfrac{0,2}{0,1}=2\left(M\right)\)

-a/Viết phương trình chữ của phản ứng:
Kẽm + Axit Clohidric -> Kẽm Clorua + Khí hidro
\(Zn+2HCl->ZnCl_2+H_2\)
b/Viết công thức về khối lượng của phản ứng
\(m_{Zn}+m_{HCl}=m_{ZnCl_{ }}+m_H\)
c/Cho biết khối lượng của Zn và HCI đã phản ứng là 6,5g và 7,3g,khối lượng của ZnCl2 là 13,6g.Hãy tính khối lượng của khí hidro bay lên
- Khối lượng của khí hidro bay lên là:
\(m_{H_2}=\left(6,5+7,3\right)-13,6=0,2\left(g\right)\)

\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,4
0,1 0,2
0 0,2 0,1 0,1
\(a,V_{H_2}=0,1.22,4=2,24\left(l\right)\\ b,m_{dd}=6,5+0,4.36,5+50-0,1.2=70,9\left(g\right)\\ C\%_{ZnCl_2}=\dfrac{0,1.136}{70,9}.100\%=19,18\%\)
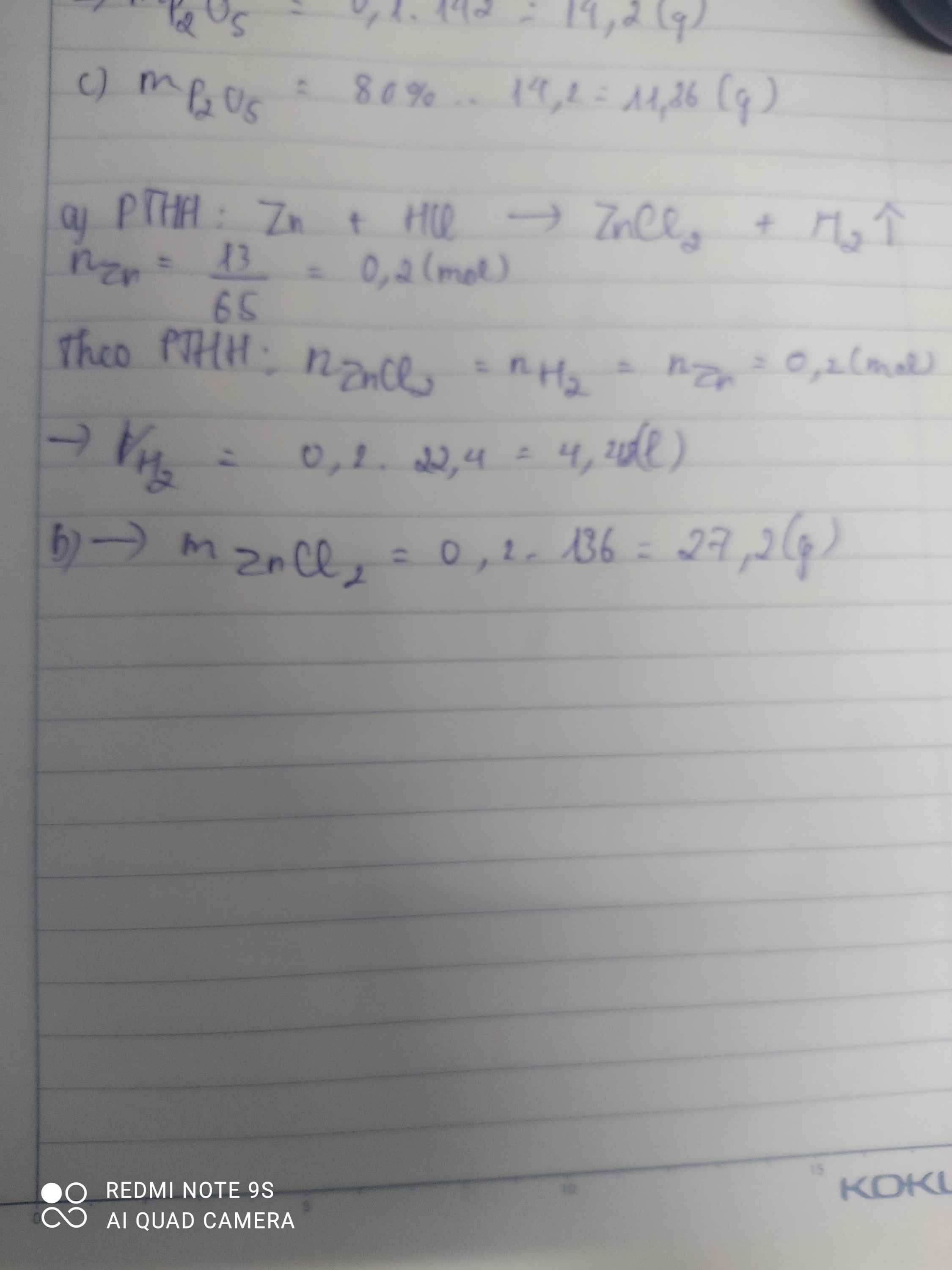
Đáp án C