Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B.
Các thí nghiệm có phản ứng oxi hóa – khử xảy ra bao gồm: (1), (3), (5), (6), (8)
(1) 3 F e 2 + + 4 H + + N + 5 O 3 - → 3 F e 3 + + N + 2 O + 2 H 2 O
(2) C u 0 + F e + 3 N O 3 3 → C u + 2 N O 3 2 + F e + 2 N O 3 2
(5) 10 F e + 2 S O 4 + 2 K M n + 7 O 4 + 8 H 2 S O 4 → 5 F e 2 + 3 S O 4 3 + K 2 S O 4 + 2 M n + 2 S O 4 + 8 H 2 O
(6) F e + 2 N O 3 2 + A g + N O 3 → F e + 3 N O 3 3 + A g 0
(8) 6 F e + 2 S O 4 + 2 C r + 6 O 3 + 6 H 2 S O 4 → 3 F e 2 + 3 S O 4 3 + C r 2 + 3 S O 4 3 + 6 H 2 O

Ta có: $n_{Al}=n_{Fe}=0,1(mol)$
Sau phản ứng thì Al hết, Fe chưa phản ứng hoặc còn dư
Gọi số mol $Cu(NO_3)_2 và $AgNO_3$ lần lượt là a;b
Ta có: $64a+108b=28$
Bảo toàn e toàn bộ quá trình ta có: $2a+b=0,4$
Giải hệ ta được $a=0,1;b=0,2$
$\Rightarrow [Cu(NO_3)_2]=1M;[AgNO_3]=2M$
\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0.05\left(mol\right)\)
\(n_{Al}=n_{Fe}=a\left(mol\right)\)
\(\Rightarrow a=\dfrac{8.3}{27+56}=0.1\)
\(n_{AgNO_3}=x\left(mol\right),n_{Cu\left(NO_3\right)_2}=y\left(mol\right)\)
\(m_{cr}=108x+64y=28\left(1\right)\)
Bảo toàn e :
\(x+2y=0.4\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.2,y=0.1\)
\(C_{M_{AgNO_3}}=\dfrac{0.2}{0.1}=2\left(M\right)\)
\(C_{M_{Cu\left(NO_3\right)_2}}=\dfrac{0.1}{0.1}=1\left(M\right)\)

Giải thích:
Định hướng tư duy giải
(1) CO2 + NaAlO2 + H2O → Al(OH)3 + NaHCO3
(2) AlCl3 + 3NH3 + 3H2O → Al(OH)3 + 3NH4Cl
(3) AlCl3 + 4NaOHdư → NaAlO2 + 3NaCl + 2H2O
(4) Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag

(6) Còn có Cu dư
Đáp án D

Đáp án D
(1) CO2 + NaAlO2 + H2O ->Al(OH)3 + NaHCO3
(2) AlCl3 + 3NH3 + 3H2O ->Al(OH)3 + 3NH4Cl
(3) AlCl3 + 4NaOHdư ->NaAlO2 + 3NaCl + 2H2O
(4) Fe(NO3)2 + AgNO3 ->Fe(NO3)3 + Ag
(5) 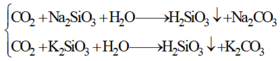
(6) Còn có Cu dư
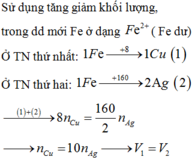
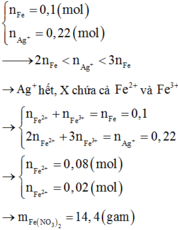
Cho bột Fe vào dung dịch AgNO3 dư, sau khi kết thúc thí nghiệm thu được dung dịch X gồm:
A. Fe(NO3)2, H2O B. Fe(NO3)2, AgNO3
C. Fe(NO3)3, AgNO3 D. Fe(NO3)2, Fe(NO3)3, AgNO3
HT