Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

4HCl + Mn O 2 → Mn Cl 2 + 2 H 2 O + Cl 2
1 mol Mn O 2 → 1 mol Cl 2
a/87 mol Mn O 2 → a/87 mol Cl 2
16HCl + 2KMn O 4 → 2KCl + 2Mn Cl 2 + 8 H 2 O + 5 Cl 2
2 mol KMn O 4 → 5 mol Cl 2
a/158 mol KMn O 4 → a/63,2 mol
Có a/63,2 > a/87
Chọn KMn O 4 đều chế được nhiều clo hơn

4HCl + Mn O 2 → Mn Cl 2 + 2 H 2 O + Cl 2
a mol Mn O 2 → a mol Cl 2
16HCl + 2KMn O 4 → 2KCl + 2Mn Cl 2 + 8 H 2 O + 5 Cl 2
2 mol KMn O 4 → 5 mol Cl 2
a mol KMn O 4 → 5a/2 mol
Chọn KMn O 4 đều chế được nhiều clo hơn

2KMnO4+16HCl--->2KCl+MnCl2+5Cl2+8H2O(1)
MnO2+4HCl-->MnCl2+Cl2+2H2O(2)
1)gọi khối lượng của 2 chất là a(g)
nKMnO4=\(\frac{a}{158}\)(mol)
nMnO2=\(\frac{a}{87}\)(mol)
theo pthh(1): nCl2=\(\frac{5}{2}\)nKMnO4=\(\frac{5}{2}\).\(\frac{a}{158}\)=\(\frac{5a}{316}\)(mol)
theo pthh(2): nCl2=nMnO2=nMnO2=\(\frac{a}{87}\)
vì \(\frac{5a}{316}\)>\(\frac{a}{87}\) nên chọn chất KMnO4 là điều chế được nhiều clo nhất
2)gọi số mol của 2 chất là x mol
theo pthh(1): nCl2=\(\frac{5}{2}\) nKMnO4=\(\frac{5x}{2}\)(mol)
theo pthh(2): nCl2=nMnO2=x(mol)
vì \(\frac{5x}{2}\)>x nên dùng KMnO4 là điều chế được nhiều clo nhất
1.
mKMnO4 = mMnO2 = x gam
—> nKMnO4 = x/158
nMnO2 = x/87
2KMnO4 + 16HCl —> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
x/158…………………………………….....5x/316
MnO2 + 4HCl —> MnCl2 + Cl2 + 2H2O
x/87……………………………x/87
Vì 5x/316 > x/87 —> Dùng KMnO4 thu nhiều Cl2 hơn.

a) 2KMnO4 +16HCl --> 2KCl+2MnCl2 +5Cl2+8H2O
1 mol 2,5 mol
MnO2 + 4HCl --> MnCl2 +Cl2 +2H2O
1mol 1 mol
quan sát 2 phương trình ta thấy để thu cùng 1 lượng Cl2 thì dung KMnO4 lợi hơn
b)
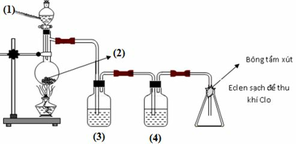
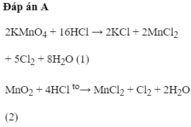

a) - Nếu dùng KMnO4:
2 KMNO4 + 16 HCl = 2 KCl + 2 MnCl2 + 8 H2O + 5 Cl2 (1)
- Nếu dùng MnO2:
MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O (2)
Theo pt ta thấy (1) tạo ra 5Cl2 còn pư (2) chỉ tạo 1Cl2, chứng tỏ (1) tạo ra nhiều clo hơn (2).
b) giả sử số mol của KMnO4 và MnO2 là 0.2 mol
2 KMNO4 + 16 HCl = 2 KCl + 2 MnCl2 + 8 H2O + 5 Cl2 (1)
0.2.................................................................................0.5
MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O (2)
0.2........................................0.2
Ta thấy số mol Cl2 ở (1) lớn hơn số mol Cl2 ở (2), suy ra pư (1) tạo nhiều clo hơn (2).
c) Từ (1) và (2) ta thấy:
Số mol HCl (1) lớn gấp 4 lần số mol HCl ở (2), suy ra ở pư (1) tiêu tốn HCl hơn pư (2).
Để thu được nhiều Clo hơn ta nên dùng pư (1) , còn muốn tiết kiệm HCl ta nên dùng MnO2.