Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
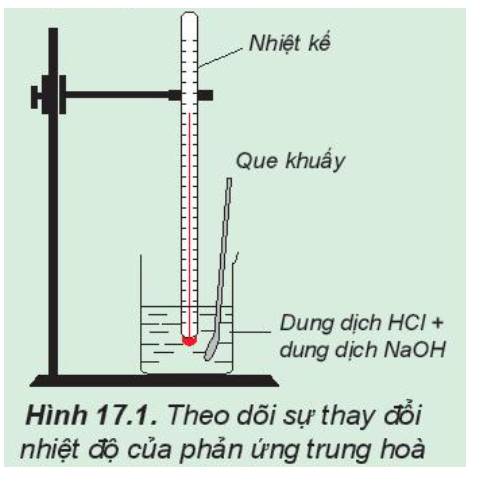
Phản ứng hóa học: NaOH + HCl → NaCl + H2O
Nhiệt độ đo được (HCl) lúc ban đầu thấp hơn so với nhiệt độ sau phản ứng
=> Phản ứng trung hòa là phản ứng tỏa nhiệt
2.
Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ sau phản ứng vẫn tăng nhưng tăng ít hơn so với thí nghiệm trên.

1)
nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol. 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = CM(MnCl2) = CM(NaClO) = 0,8 /0,5 = 1,6 mol/l
CM(NaOH)dư = (2. 1,6)/0,5 = 0,8 mol/l
câu 3
nNaCl = = 0,1 mol;
=
= 0,2 mol
a) Phương trình hóa học của phản ứng:
NaCl + AgNO3 → AgCl↓ + NaNO3
0,1 mol 0,1 mol 0,1 mol 0,1 mol
mAgCl = 143,5 x 0,1 = 14,35g
b) Vdd = 300 + 200 = 500 ml
= 0,2 - 0,1 = 0,1 mol
=
=
= 0,2 mol/l

Câu 5 : Cho hỗn hợp hai muối MgCO3 và CaCO3 tan trong dung dịch HCl vừa đủ tạo ra 2,24 lít khí đktc . Số mol của 2 muối cacbonat ban đầu là ?
| MgCO3 | → | MgO | + | CO2 |
CaCO3-->CaO+CO2
n hỗn hợp khí =2,24\22,4 =0,1 mol
=>nhh 2muối =0,1 mol

a: Tốc độ phản ứng tăng lên do bề mặt tiếp xúc tăng lên
b: Tốc độ phản ứng giảm xuống do nồng độ giảm
c: Tốc độ phản ứng tăng lên do nhiệt độ tăng

Những câu như này không nên đưa lên CHH nha các CTV
Bài 1
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
0,2 ________________________ 0,2_____
\(n_{MnO2}=\frac{17,4}{55+32}=0,2\)
\(\rightarrow V_{Cl2}=0,2.22,4=4,48\left(l\right)\)
\(PTHH:2NaOH+Cl_2\rightarrow NaClO+NaCl+H_2O\)
Ban đầu ____0,2 ___0,45
Phứng_______0,2_____0,4
Sau phứng _0__________0,05 ____ 0,4 ________ 0,4
Đổi 200ml=0,2l
\(n_{NaOH}=0,2.2,25=0,45\left(mol\right)\)
\(CM_{NaClO}=CM_{NaCl}=\frac{0,4}{0,2}=2M\)
\(CM_{NaOH_{du}}=\frac{0,05}{0,2}=0,25M\)
\(PTHH:3Cl_2+2Fe\rightarrow2FeCl_3\)
Ban đầu __0,2___ 0,09____________
Phứng___0,135__ 0,09_______
Sau phứng___0,065___ 0______0,09
\(n_{Fe}=\frac{5,04}{56}=0,09\left(mol\right)\)
\(n_{FeCl3_{tt}}=0,09.8-\%=0,072\)
\(m_{FeCl_3}=0,072.\left(56+35,5.3\right)=11,7\left(g\right)\)
Bài 2:
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
0,15_______________________________ 0,375_______
\(n_{KMnO4}=\frac{23,7}{39+55+16.4}=0,15\left(mol\right)\)
\(\rightarrow V_{Cl2}=0,375.22,4=8,4\left(l\right)\)
\(PTHH:6KOH+3Cl_2\rightarrow KClO_3+5KCl+3H_2O\)
Ban đầu __0,375____ 0,4________________________
Phứng ___0,2 ______0,4________________________________
Sau phứng__ 0,175 __ 0 ___ 1/15____ 1/3
Đổi 200ml =0,2l
\(n_{KOH}=0,2.2=0,4\left(mol\right)\)
\(CM_{Cl2_{Du}}=\frac{0,175}{0,5}=0,4375M\)
\(CM_{KClO3}=\frac{\frac{1}{15}}{0,4}=\frac{1}{6}M\)
\(CM_{KCl}=\frac{\frac{1}{3}}{0,4}=\frac{5}{6}M\)
Gọi kim loại là R
\(3Cl_2+2R\rightarrow2RCl_3\)
0,375___0,25________
\(M_R=\frac{6,75}{0,25}=27\left(Al\right)\)
Bài 3 :
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
0,2____________________________________ 0,5________
\(n_{KMnO4}=\frac{31,6}{39+55+16.4}=0,2\left(mol\right)\)
\(\rightarrow V_{Cl2}=0,5.22,4=11,2\left(l\right)\)
\(PTHH:2NaOH+Cl_2\rightarrow aClO+NaCl+H_2O\)
Ban đầu ___0,5 ____0,4_______________________________
Phứng___ 0,2______ 0,4_____________________
Sau phứng__0,3 _____0 _____0,2 _____0,2____________
Đổi 200ml=0,2l
\(n_{NaOH}=0,2.2=0,4\left(mol\right)\)
\(CM_{NaClO}=CM_{NaCl}=\frac{0,2}{0,2}=1M\)
\(CM_{Cl2_{Du}}=\frac{0,3}{0,2}=1,5M\)
\(PTHH:Cl_2+Ca\rightarrow CaCl_2\)
Ban đầu__0,5____0,6________
Phứng__0,5____0,5 ______________
Sau phứng _0,1___ 0 _____ 0,5
\(n_{Ca}=\frac{24}{40}=0,6\left(mol\right)\)
\(m_{Ca_{lt}}=0,5.\left(40+71\right)=55,5\left(g\right)\)
\(\rightarrow H=\frac{44,4}{55,4}.100=80\%\)

9): n(CO2) = 4,48/22,4 = 0,2mol
Số mol mỗi chất trong hỗn hợp dung dịch ban đầu:
n(Na2CO3) = 0,5.0,2 = 0,1mol; n(NaOH) = 0,75.0,2 = 0,15mol
Khi cho CO2 vào dung dịch chứa Na2CO3 và NaOH thứ tự các phản ứng xảy ra:
2NaOH + CO2 → Na2CO3 + H2O
0,15 0,075 0,075
CO2 + Na2CO3 + H2O → 2NaHCO3
0,125 0,125 0,25
Số mol Na2CO3 có trong dung dịch X:
n(Na2CO3) = 0,1 + 0,075 - 0,125 = 0,05mol
Cho dung dịch BaCl2 dư vào dung dịch X:
Na2CO3 + BaCl2 → BaCO3 + 2NaCl
0,05 0,05
Khối lượng kết tủa thu được: m(BaCO3) = 0,05.197 = 9,85gam
1) Dung dịch A chứa CO32- (x mol) và HCO3- (y mol)
CO32- + H+ —> HCO3-
x…………x………….x
HCO3- + H+ —> CO2 + H2O
x+y…….0,15-x
Dung dịch B tạo kết tủa với Ba(OH)2 nên HCO3- dư, vậy nCO2 = 0,15 – x = 0,045 —> x = 0,105
HCO3- + OH- + Ba2+ —> BaCO3 + H2O
—> nBaCO3 = (x + y) – (0,15 – x) = 0,15 —> y = 0,09
—> m = 20,13 gam
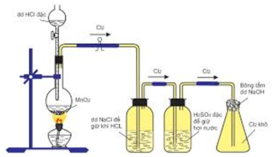

Chọn đáp án D
D sai vì nếu thay NaCl bằng KOH thì C l 2 sinh ra sẽ phản ứng với KOH, không thu được khí clo.