
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

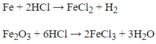

PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
a) Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_{Fe}\)
\(\Rightarrow m_{Fe}=0,2\cdot56=11,2\left(g\right)\) \(\Rightarrow m_{Fe_2O_3}=16\left(g\right)\)
b+c) Ta có: \(\left\{{}\begin{matrix}n_{Fe}=0,2\left(mol\right)\\n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{HCl}=2n_{Fe}+6n_{Fe_2O_3}=1\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{36,5}{20\%}=182,5\left(g\right)\)
Mặt khác: \(n_{FeCl_2}=0,2\left(mol\right)=n_{H_2}=n_{FeCl_3}\) \(\Rightarrow\left\{{}\begin{matrix}m_{FeCl_2}=0,2\cdot127=25,4\left(g\right)\\m_{FeCl_3}=0,2\cdot162,5=32,5\left(g\right)\\m_{H_2}=0,2\cdot2=0,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{dd}=m_{hhA}+m_{ddHCl}-m_{H_2}=209,3\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{25,4}{209,3}\cdot100\%\approx12,14\%\\C\%_{FeCl_3}=\dfrac{32,5}{209,3}\cdot100\%\approx15,53\%\end{matrix}\right.\)
\(n_{H2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O|\)
1 6 2 3
0,1 0,6 0,2
a) \(n_{Fe}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
\(m_{Fe2O3}=27,2-11,2=16\left(g\right)\)
b) Có : \(m_{Fe2O3}=16\left(g\right)\)
\(n_{Fe2O3}=\dfrac{16}{160}=0,1\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,4+0,6=1\left(mol\right)\)
⇒ \(m_{HCl}=1.36,5=36,5\left(g\right)\)
\(m_{ddHCl}=\dfrac{36,5.100}{20}=182,5\left(g\right)\)
c) \(n_{FeCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{FeCl2}=0,2.127=25,4\left(g\right)\)
\(n_{FeCl3}=\dfrac{0,6.2}{6}=0,2\left(mol\right)\)
⇒ \(m_{FeCl3}=0,2.162,5=32,5\left(g\right)\)
\(m_{ddspu}=27,2+182,5-\left(0,2.2\right)=209,3\left(g\right)\)
\(C_{FeCl2}=\dfrac{25,4.100}{209,3}=12,14\)0/0
\(C_{FeCl3}=\dfrac{32,5.100}{209,3}=15,53\)0/0
Chúc bạn học tốt

Gọi số mol Fe, Al là a,b
Khối lượng kim loại không tan là khối lượng của Cu
=> 56a + 27b = 9,08-2,4 = 6,68(g)
\(n_{H_2}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
______a------------------------>a
2Al + 6HCl --> 2AlCl3 + 3H2
_b------------------------->1,5b
=>a + 1,5b = 0,16 (mol)
=> a = 0,1; b = 0,04
=> mFe = 0,1.56 = 5,6 (g)
=> mAl = 0,04.27 = 1,08(g)

\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
___________________0,3<----0,3____(mol)
=> mMgCl2 = 0,3.95 = 28,5 (g)

2Fe + 3 Cl 2 → t ° 2Fe Cl 3 ( M FeCl 3 = 162,5 gam)
Cu + Cl 2 → t ° Cu Cl 2
Fe + 2HCl → Fe Cl 2 + H 2 ( M FeCl 2 = 127 gam)
n Fe = x mol
Theo đề bài và phương trình hóa học trên ta có:
127x = 25,4 => 0,2 mol
162,5x + 135y = 59,5. Thay x = 0,2 vào phương trình, ta có:
32,5 + 135y = 59,5 => y = 0,2
m FeCl 3 = 0,2 x 162,5 = 32,5g
m CuCl 2 = 0,2 x 135 = 27g
% m FeCl 3 = 32,5 : (32,5 + 27).100% = 54,62%
% m CuCl 2 = 100% - 54,62% = 45,38%

\(n_{Al}=a\left(mol\right)\)
\(n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=19.3\left(g\right)\left(1\right)\)
\(n_{H^+}=0.2\cdot2+0.2\cdot2.25\cdot2=1.3\left(mol\right)\)
\(2Al+6H^+\rightarrow2Al^{3+}+3H_2\)
\(Fe+2H^+\rightarrow Fe^{2+}+H_2\)
\(n_{H^+}=3a+2b=1.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.3,b=0.2\)
\(\%Al=\dfrac{0.3\cdot27}{19.3}\cdot100\%=41.96\%\)
\(\%Fe=58.04\%\)
\(b.\)
\(n_{H_2}=\dfrac{1}{2}n_{H^+}=0.65\left(mol\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=19.3+0.4\cdot36.5+0.45\cdot98-0.65\cdot2=76.7\left(g\right)\)