Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nhỏ dung dịch HCl vào dung dịch X:
Các phương trình hóa học:
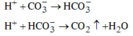
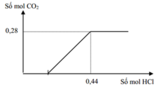
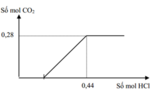
Tại 0,28 mol CO2 và 0,44 mol HCl thì lượng khí bắt đầu không đổi, chứng tỏ H+ phản ứng đủ với các ion ![]()
Sơ đồ phản ứng:
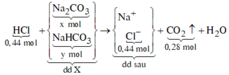
![]()
![]()
![]()
![]()
![]()
![]()
![]()
*Nhỏ từ từ 200ml dung dịch HCl 0,8M và H2SO4 aM vào 200ml dung dịch X:
Số mol các chất là: ![]()
![]()
Sơ đồ phản ứng:
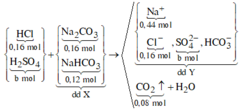
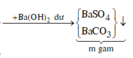
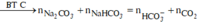
![]()

![]()
![]()
![]()
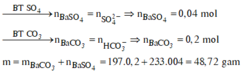
Đáp án C.

Chọn C.
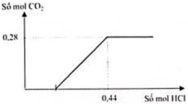
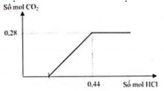
- Xét đồ thị :
+ Tại vị trí không thoát khí thì : n C O 3 2 - = n H + - n C O 2 = 0 , 16 m o l ⇒ n H C O 3 - = n C O 2 - n C O 3 2 - = 0 , 12 m o l
+ Vậy dung dịch X chứa 0,16 mol Na2CO3 và 0,12 mol NaHCO3
- Khi cho dung dịch X tác dụng với dung dịch chứa HCl (0,16 mol) và H2SO4 (0,2a mol) thì :
n H C l + n H 2 S O 4 = n C O 2 + n C O 3 2 - → 0 , 16 + 2 . 0 , 2 a = 0 , 16 + 0 , 08 ⇒ a = 0 , 2
- Cho Y tác dụng với Ba(OH)2 dư thì: n B a C O 3 = n C O 3 2 - + n H C O 3 - - n C O 2 = 0 , 2 m o l và n B a S O 4 = n H 2 S O 4 = 0 , 04 m o l .
Vậy m k t u a = 197 n B a C O 3 + 233 n B a S O 4 = 48 , 72 g a m

Đáp án B
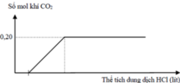
Trong 100ml X chứa 0,04 mol NaHCO3 và 0,06 mol Na2CO3.
Trong 100 ml Y chứa 0,1x mol HCl và 0,1x mol H2SO4.
Cho từ từ X vào Y thu được 0,075 mol CO2.
Khi cho Xvào Y thì hai muối trong X phản ứng theo tỉ lệ mol







Đáp án C