Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)

\(M_A=18.2=36\left(g/mol\right)\)
Áp dụng sơ đồ đường chéo:
\(\dfrac{n_{CO}}{n_{CO_2}}=\dfrac{44-36}{36-28}=\dfrac{1}{1}\)
\(n_{CaCO_3}=\dfrac{40}{100}=0,4\left(mol\right)\)
Đặt CTHH của oxit sắt là \(Fe_xO_y\)
PTHH:
\(Fe_xO_y+yCO\xrightarrow[]{t^o}xFe+yCO_2\) (1)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\) (2)
Theo PT (2): \(n_{CO_2}=n_{CaCO_3}=0,4\left(mol\right)\)
\(\Rightarrow n_{CO\left(d\text{ư}\right)}=n_{CO_2}=0,4\left(mol\right)\)
Theo PT (1): \(n_{Fe_xO_y}=\dfrac{1}{y}.n_{CO_2}=\dfrac{0,4}{y}\left(mol\right);n_{CO\left(p\text{ư}\right)}=n_{CO_2}=0,4\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{23,2}{\dfrac{0,4}{y}}=86y\left(g/mol\right)\\ \Rightarrow56x+16y=86y\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
=> CT của oxit là Fe3O4
V = (0,4 + 0,4).22,4 = 17,92 (l)

bạn ơi, cho mình hỏi làm sao lập được bảng đó vậy? chỉ mình với

Ta có: nCO = 0,2 (mol)
- Hỗn hợp khí sau pư gồm: CO dư và CO2.
Gọi: \(\left\{{}\begin{matrix}n_{CO\left(pư\right)}=x\left(mol\right)\\n_{CO\left(dư\right)}=y\left(mol\right)\end{matrix}\right.\) ⇒ x + y = 0,2 (1)
\(CO_{\left(pư\right)}+O_{\left(trongoxit\right)}\rightarrow CO_2\)
x________x__________x (mol)
\(\Rightarrow\dfrac{44x+28y}{x+y}=20.2\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,15\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
⇒ nO (trong oxit) = 0,15 (mol)
⇒ nFe (trong oxit) = 8 - 0,15.16 = 5,6 (g) ⇒ nFe = 0,1 (mol)
Gọi CTHH của oxit là FexOy.
\(\Rightarrow\dfrac{x}{y}=\dfrac{0,1}{0,15}=\dfrac{2}{3}\)
Vậy: CTHH cần tìm là Fe2O3.
Gọi CTHH của oxit là $R_2O_n$
$R_2O_n + nCO \xrightarrow{t^o} 2R + nCO_2$
Hỗn hợp khí sau phản ứng gồm $CO$ dư (a mol) và $CO_2(b\ mol)$
Suy ra :
$a + b = \dfrac{4,48}{22,4} = 0,2$
$\dfrac{28a + 44b}{a + b} = 20.2$
Suy ra : a = 0,05 ; b = 0,15
Theo PTHH : $n_{oxit} = \dfrac{n_{CO_2}}{n} = \dfrac{0,15}{n}(mol)$
$\Rightarrow \dfrac{0,15}{n}.(2R + 16n) = 8$
$\Rightarrow R = \dfrac{56}{3}n$
Với n = 3 thì R = 56(Fe)
Vậy oxit là $Fe_2O_3$

\(Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2\\ n_{CO} = \dfrac{4,48}{22,4} = 0,2(mol)\\ n_{CO\ pư} = a ; n_{CO\ dư} = b\\ \Rightarrow a + b = 0,2(1)\\ n_{CO_2} = a(mol)\\ m_X = 44a + 28b = (a + b).2.20 = 0,2.2.20 = 8(2)\\ (1)(2)\Rightarrow a = 0,15 ; b = 0,05\\ \%V_{CO_2} = \dfrac{0,15}{0,2}.100\% = 75\%\\ n_{Oxit} = \dfrac{n_{CO_2}}{y}=\dfrac{0,15}{y}(mol)\\ \)
\(\Rightarrow \dfrac{0,15}{y}(56x + 16y) = 8\\ \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}\)
Vậy oxit là Fe2O3

(a) Vì khi cho chất rắn thu được sau phản ứng với CO tác dụng với dung dịch HCl tạo ra khí H2 nên R phải là kim loại đứng sau Al và đứng trước hidro trong dãy hoạt động hóa học. Đặt công thức oxit của R là RxOy.
CuO + CO → Cu + CO2
a a
RxOy + yCO → xR + y CO2
c xc
Al2O3 + 6HCl → RCln + n/2 H2
xc nxc xc nxc/2
Đạt các mol CuO, Al2O3, RxOy trong 6,1 g hỗn hợp A là a,b,c. Có
80a + 102b+ (xMr + 16y)c = 6,1
1,28 + 102b + Mrxc = 4,82
64a = 1,28
6b + nxc = 0,15
nxc/2 = 0,045
=> a = 0,02
=> nxc = 0,09
b = -0,01
Mr = 28n
=> n = 2 , Mr = 56, R là Fe
xc = 0,45 => yc = 0,06
x/y = 0,045/0,06 = 3/4
=> x = 3, y = 4 CT oxit = Fe2O3
bạn ơi bài trên giải sai thì phải
sao al2o3+có lại được rcln+h2

Cho hỏi chỗ sơ đồ đường chéo 4 và 12 là như nào đấy ạ .___.
Còn cả chỗ suy ra 42x-28y=0

a) FexOy+yCO→xFe+yCO2
b) +) Quy đổi 8g oxit sắt thành 8g (Fe; O). Khi đó, xảy ra phản ứng với CO
CO + O 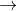 CO2
CO2
=> nCO (phản ứng) = nCO2
+) Lại có: M khí sau phản ứng = 2.d khí/H2 = 40 (g) ≠ MCO2
=> CO còn dư và O phản ứng hết
=> n hh sau = nCO ban đầu =  = 0,2 (mol)
= 0,2 (mol)
=> ∆m = m hh sau – mCO bđ = m Oxi (hh rắn) = 40.0,2 – 28.0,2 = 2,4 (g)
=> nCO2 = nO = 0,15 (mol)
=> mFe = 8 – 2,4 = 5,6 (g)
=> nFe = 0,1 (mol) ; nO = 0,15 (mol)
=> nFe : nO = 2 :3
=> CTPT oxit sắt là Fe2O3
Mặt khác, %V CO2/hh khí sau phản ứng = 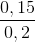 . 100% = 75%
. 100% = 75%
a)FexOy+yCO→xFe+yCO2
b)+) Quy đổi 8g oxit sắt thành 8g (Fe; O). Khi đó, xảy ra phản ứng với CO
CO + O 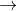 CO2
CO2
=> nCO (phản ứng) = nCO2
+) Lại có: M khí sau phản ứng = 2.d khí/H2 = 40 (g) ≠ MCO2
=> CO còn dư và O phản ứng hết
=> n hh sau = nCO ban đầu =  = 0,2 (mol)
= 0,2 (mol)
=> ∆m = m hh sau – mCO bđ = m Oxi (hh rắn) = 40.0,2 – 28.0,2 = 2,4 (g)
=> nCO2 = nO = 0,15 (mol)
=> mFe = 8 – 2,4 = 5,6 (g)
=> nFe = 0,1 (mol) ; nO = 0,15 (mol)
=> nFe : nO = 2 :3
=> CTPT oxit sắt là Fe2O3
Mặt khác, %V CO2/hh khí sau phản ứng = 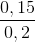 . 100% = 75%
. 100% = 75%


\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Có nO(mất đi) = nCO2 = 0,15 (mol)
=> mrắn sau pư = 26,4 - 0,15.16 = 24(g)