Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
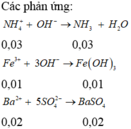
Khi cho NaOH, hay Ca(OH)2 dư tác dụng 1/2 dd X, đều xảy ra phản ứng:
HCO3- + OH- → CO32- + H2O. (1)
Ca2+ + CO32- → CaCO3. (2)
Khi tác dụng Ca(OH)2 dư thì do Ca2+ và OH- dư nên n(↓ phần 2) = n(HCO3-) = 4 , 5 100 = 0,045 mol.
Khi tác dụng NaOH dư, do OH- dư nên HCO3- phản ứng hết. với n(HCO3-) = 0,045. Trong khi n(↓ phần 1) = 2 100 = 0,02 < 0,045
⇒ kết tủa tính theo Ca2+ với n(Ca2+) = n (↓ phần 1) = 0,02 mol.
Bảo toàn điện tích (trong 1/2 dd) → n(Na+) + 2n(Ca2+)= n(HCO3-) + n(Cl-)
=> n(Na+) = 0,045 + 0,035- 0,02.2= 0,04 mol
Khi đun sôi thu được muối chứa Na+( tính trong 1/2 dd):
2HCO3- → CO32- + CO2+ H2O
0,04 mol Na+; 0,02 mol Ca2+; 0,035 mol Cl-; 0 . 045 2 CO32-.
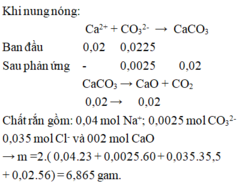
Khi nung nóng:
Ca2+ + CO32- → CaCO3
Ban đầu 0,02 0,0225
Sau phản ứng - 0,0025 0,02
CaCO3 → CaO + CO2
0,02 → 0,02
Chất rắn gồm: 0,04 mol Na+; 0,0025 mol CO32-; 0,035 mol Cl- và 002 mol CaO
→ m =2(0,04.23 + 0,0025.60 + 0,035.35,5 + 0,02.56) = 6,865 gam.

Nhận thấy lượng kết tủa thu được khi cho vào NaOH nhỏ hơn khi cho X vào Ba(OH)2
→ n(Ba2+) < n(HCO3-)
Trong phần 1 → n(Ba2+) = 9,85 : 197 = 0,05 mol
Trong phần 2 → n(HCO3-) = 15,76 : 197 = 0.08 mol
Bảo toàn điện tích → n(Na+) = 0,08 + 0,12 – 0,05.2 = 0,1 mol
Khi đun sôi thu được muối chứa Na+ : 0,1 mol, Ba2+ : 0,08 mol, Cl- : 0,12 mol, CO3- : 0,04 mol
→ m = 2.(0,1.23 + 0,05.137 + 0,12.35,5 + 0,04.60) = 31,62 gam
→ Đáp án C




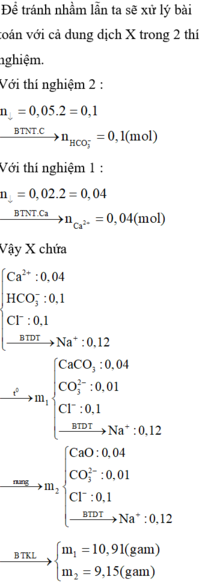
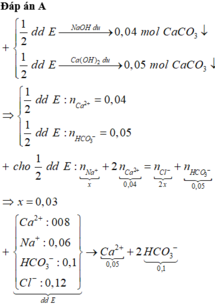

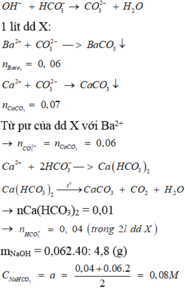
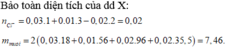
Đáp án C