Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2C_8H_{18}+25O_2\xrightarrow{t^o}16CO_2+18H_2O\\ a,n_{O_2}=\dfrac{500}{5.16}=6,25(mol)\\ \Rightarrow n_{C_8H_{18}}=\dfrac{2}{25}.6,25=0,5(mol)\\ \Rightarrow V_{C_8H_{18}}=0,5.22,4=11,2(l)\\ b,n_{C_8H_{18}}=\dfrac{240}{22,4}=\dfrac{75}{7}(mol)\\ \Rightarrow n_{O_2}=\dfrac{1875}{14}(mol)\\ \Rightarrow V_{O_2}=\dfrac{1875}{14}.22,4=3000(l)\)

Giả sử khí được đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
\(n_A=\dfrac{2}{1}=2\left(mol\right)\)
\(n_{O_2}=\dfrac{9}{1}=9\left(mol\right)\)
\(n_{CO_2}=\dfrac{6}{1}=6\left(mol\right)\)
\(n_{H_2O}=\dfrac{8}{1}=8\left(mol\right)\)
Bảo toàn C: nC(A) = 6 (mol)
Bảo toàn H: nH(A) = 16 (mol)
Bảo toàn O: \(n_{O\left(A\right)}=6.2+8.1-9.2=2\left(mol\right)\)
Số nguyên tử C là \(\dfrac{6}{2}=3\) (nguyên tử)
Số nguyên tử H là \(\dfrac{16}{2}=8\) (nguyên tử)
Số nguyên tử O là \(\dfrac{2}{2}=1\) (nguyên tử)
=> CTPT: C3H8O

a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2. Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
VO2 = 2 . 2 = 4 lít.
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
VCO2 = 0,15 . 22,4 = 3,36 lít.
c) Tỉ khối của khí metan và không khí là:
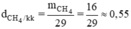
Vậy khí metan nhẹ hơn không khí 0,55.

Các khí đo ở cùng điều kiện nhiệt độ , áp suất thì tỉ lệ về thể tích cũng là tỉ lệ về số mol
C8H18 + 25/2O2 --> 8CO2 + 9H2O
Theo pt : 1 25/2 8 9 (lít)
Theo đề bài 8 <------100
Theo đề bài 240 ------> 3000
Vậy thể tích khí C8H18 cháy trong 500l không khí tức 100 lít Oxi là 8 lít,
Thể tích oxi cần dùng để đốt cháy hết 240 lít C8H18 là 3000 lít

a) PTHH: 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
=> \(V_{O_2}=\dfrac{5}{2}V_{C_2H_2}=\dfrac{5}{2}.4=10\left(l\right)\)
b) \(\left\{{}\begin{matrix}n_{C_2H_2}=\dfrac{3,9}{26}=0,15\left(mol\right)\\n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\end{matrix}\right.\)
LTL: \(\dfrac{0,15}{2}< \dfrac{0,4}{5}\) => O2 dư
=> \(\left\{{}\begin{matrix}n_{CO_2}=0,15.2=0,3\left(mol\right)\\n_{O_2\left(pư\right)}=\dfrac{5}{2}.0,15=0,375\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow M_{hh}=\dfrac{0,3.44+\left(0,4-0,375\right).32}{0,3+0,4-0,375}=\dfrac{560}{13}\left(\dfrac{g}{mol}\right)\)
=> dhh/H2 = \(\dfrac{\dfrac{560}{13}}{2}=\dfrac{280}{13}\)

Theo gt ta có: $n_{H_2}=0,75(mol)$
a, $2H_2+O_2\rightarrow 2H_2O$
Ta có: $n_{O_2}=0,5.n_{H_2}=0,375(mol)\Rightarrow V_{O_2}=8,4(l)\Rightarrow V_{kk}=42(l)$
b, $2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2$
Ta có: $n_{KMnO_4}=2.n_{O_2}=0,75(mol)\Rightarrow m_{KMnO_4}=118,5(g)$
a)
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ V_{O_2} = \dfrac{V_{H_2}}{2} = \dfrac{16,8}{2} = 8,4(lít)\\ V_{không\ khí} = \dfrac{8,4}{20\%} = 42(lít)\)
b)
\(n_{O_2} = \dfrac{8,4}{22,4} = 0,375(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,75(mol)\\ \Rightarrow m_{KMnO_4} = 0,75.158 = 118,5(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,25(mol)\\ \Rightarrow m_{KClO_3} = 0,25.122,5 = 30,625(gam)\)

\(m_{CH_4}=0,3.16=4,8(g)\)
Bảo toàn KL: \(m_{CH_4}+m_{O_2}=m_{CO_2}+m_{H_2O}\)
\(\Rightarrow m_{O_2}=10,8+13,2-4,8=19,2(g)\\ \Rightarrow V_{O_2}=\dfrac{19,2}{32}.22,4=13,44(l)\\ \Rightarrow V_{kk}=13,44.5=67,2(l)\)

PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Ta có: \(n_{CH_4}=\dfrac{30,9875}{24,79}=1,25\left(mol\right)\)
a, \(n_{H_2O}=2n_{CH_4}=2,5\left(mol\right)\) \(\Rightarrow m_{H_2O}=2,5.18=45\left(g\right)\)
b, \(n_{O_2}=2n_{CH_4}=2,5\left(mol\right)\) \(\Rightarrow V_{O_2}=2,5.24,79=61,975\left(l\right)\)
Mà: O2 chiếm 1/5 thể tích không khí.
\(\Rightarrow V_{kk}=5V_{O_2}=309,875\left(l\right)\)

Ta có nH=5:22,4=\(\frac{25}{112}\) mol
pthh:4H+O2\(\rightarrow\)2H2O
\(\Rightarrow\)nO2= \(\frac{1}{4}.\frac{25}{112}=\frac{25}{448}\) MOL
VO2=\(\frac{25}{448}.22,4=1,25\) lít
vì VO2=\(\frac{1}{5}\)Vkk\(\Rightarrow\) 1,25.5=6,25(lít)
vậy Vkk=6,25 lít
chúc bạn học tốt like mình nha
đúng chắc chắn ko z bạn