Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n A g = 16,2/108 = 0,15 mol
Vì H = 75% nên ta có:
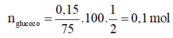
⇒ m g l u c o z o = 0,1.180 = 18g
⇒ Chọn B.

Vì H = 75% nên:
n
A
g
=
2
.
n
g
l
u
c
o
z
o
100
.
75
=
2
.
54
180
100
.
75
=
0
,
45
m
o
l
⇒ m A g = 0,45.108 = 48,6g
⇒ Chọn B.

Cu + 2H2SO4 → CuSO4 + SO2↑ + 2H2O(1)
Zn + 2H2SO4 → ZnSO4 + SO2↑ + 2H2O(2)
NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4(3)
NaOH + ZnSO4 → Zn(OH)2↓ + Na2SO4(4)
SO2 + Ba(OH)2 → BaSO3↓ + H2O(5)
SO2 + H2O → H2SO3
BaSO3 → BaO + SO2
Cu+ 2H2SO4 đặc\(\xrightarrow[]{to}\) CuSO4+ SO2+ 2H2O
Zn+ 2H2SO4 đặc\(\xrightarrow[]{to}\) ZnSO4+ SO2+ 2H2O
CuSO4+ 2NaOH\(\rightarrow\)Cu(OH)2\(\downarrow\)+ Na2SO4
ZnSO4+ 2NaOH\(\rightarrow\) Zn(OH)2\(\downarrow\)+ Na2SO4
SO2+ Ba(OH)2\(\rightarrow\) BaSO3+ H2O
2SO2+ Ba(OH)2\(\rightarrow\) Ba(HSO3)2
Ba(HSO3)\(\xrightarrow[]{to}\) BaSO3\(\downarrow\) + SO2+ H2O

n A g t o i d a = 2 n g l u c o z o = 2 . 36 180 = 0 , 4 m o l
⇒ m A g t o i d a = 43 , 2 g
⇒ Chọn D.

\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(\Rightarrow n_{H_2SO_4}=2n_{SO_2}=2\cdot0,2=0,4mol\)
\(\Rightarrow n_{SO_4^{2-}}=n_{H_2SO_4}=0,4mol\Rightarrow m_{SO_4^{2-}}=0,4\cdot96=38,4g\)
\(m=m_{SO_4^{2-}}+m_{hhX}=38,4+6,7=45,1g\)

\(\text{Bài 1. a. nHCl=4.8.10^23/6.023*10^23=0.8 mol}\)
A là FexOy
ta có FexOy+ HCl-->Muối +H2O
Bảo toàn H-->2nH2O=nH trong HCl=nHCl=0.8
-->nH2O=0.4
Bảo toàn O nO trong oxit=nO trong nước=0.4
\(\text{->mO trong oxit=6.4-->mFe=23.3-6.4=16.9-->nFe=0.3}\)
\(\text{->x/y=nFe/nO=0.3/0.4/3/4}\)
\(\text{->oxit là Fe3O4}\)
b. B là FexOy
\(\text{FexOy+ yH2-->xFe+ yH2O}\)
-->mFe=22.4-->nFe=0.4
-->x/y=0.4/0.6=2/3
--> oxit là Fe2O3
Bài 2.
\(CuO+CO\rightarrow Cu+CO2\)
\(FeO+CO\rightarrow Fe+CO2\)
Ta có :
\(\text{nH2O=0.6=nO-->mO=9.6}\)
m rắn giảm=mO từ oxit đi vào CO tạo thành CO2
mO=0.32-->nO=0.02
nH2=0.01
\(\text{Fe+2HCl-->FeCL2+H2}\)
0.01...............................0.01.......................(mol)
-->mFe=00.56-->mCu=0.32
-->nCu=0.005-->nCuO=0.005
\(\text{-->nO trong oxit sắt = 0.02-0.005=0.015}\)
-->FexOy x/y=nFe/nO=0.01/0.015=2/3
-->oxit là Fe2O3
Bài 3:
Đặt công thức kim loại là M2On
Ta có :
\(\text{nCaCO3=10/100=0.1}\)
\(\text{CO2+Ca(OH)2-->CaCO3+H2O}\)
0.1...............................0.1........................(mol)
\(\text{2M2On+nCO-->4M+nCO2}\)
0.2/n.......................0.1......................(mol)
Ta có khối lượng oxit
\(m=\frac{\left(2M+16n\right).0,2}{n}=8\)
\(\Rightarrow\text{M=12n-->M=24(Mg),n=2}\)
-->Oxit là MgO
n g l u c o z o = 1 2 . n A g = 1 2 . 32 , 4 108 = 0 , 15 m o l ⇒ m g l u c o z o = 0 , 15 . 180 = 27 g
⇒ Chọn C.