Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
Cần thật thật chú ý là trộn 3 thể tích bằng nhau các dung dịch
⇒ tạo 300 ml dung dịch X gồm 100 mL HCl 0,3M; 100 mL H2SO4 0,2M và 100 mL H3PO4 0,1M ||⇒
![]() mol.
mol.
V mL dung dịch Y gồm 2x mol NaOH và x mol Ba(OH)2
⇒ ![]() x mol.
x mol.
Phản ứng trung hòa:
![]()
⇒ 4x = 0,1 ⇒ x = 0,025 mol ⇒ V = n ÷ CM = 0,025 ÷ 0,1 = 0,25 lít ⇔ 250 mL.
⇒ chọn đáp án D.

Đáp án D
nH+ = 0,1(2. CMH2SO4 + CMHCl )= 0,02;
nNaOH = 0,1[CMNaOH + 2CMBa(OH)2] = 0,04.
H+ + OH- " H2O dư 0,02 mol OH-.
[OH-] = 0,02/(0,1+0,1) = 0,1 = 10-1.
[H+] = 10-13 ⇒ pH = 13

Đáp án A
∑ nH+ = 2nH2SO4 + nHCl = 2. 0,1.0,05 + 0,1.0,1 = 0,02 (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 0,1.0,2 + 2. 0,1.0,1 = 0,04 (mol)
H+ + OH- → H2O
0,02 → 0,02
=> nOH- dư = 0,04 – 0,02 = 0,02 (mol)
=> [OH-] = n: V = 0,02 : 0,2 = 0,01 M
pH = 14 + log(OH-) = 14 + (-1) = 13

Đáp án B
Ta có: nHCl = 0,036 mol, nHNO3 = 0,036 mol, nH2SO4 = 0,024 mol
⇒ ∑nH+ = 0,12 mol || ∑nOH– = 0,08×2×V + 0,23×V = 0,39V.
+ Vì pH = 2 ⇒ Sau pứ trung hòa nH+ dư = 102×(0,36+V) = 0,01V + 0,0036
+ Ta có: ∑nH+ = ∑nOH– + nH+ dư Û 0,12 = 0,39V + 0,01V + 0,0036.
⇔ V = 0,291 lít ⇒ nBa(OH)2 = 0,02328 mol.
+ Vì nBa2+ < nSO42– ⇒ m↓ = mBaSO4 = 0,02328×233 ≈ 5,42 gam
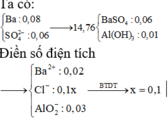
Giải thích:
nOH = 0,3 mol ; nBa2+ = 0,05 mol
nAl3+ = 0,08 mol ; nH+ = 0,2x ; nSO4 = (0,12 + 0,1x)
Vì nSO4 > nBa2+ => nBaSO4 = nBa2+ = 0,05 mol
mkết tủa = mBaSO4 + mAl(OH)3 => nAl(OH)3 = 0,06 mol < nAl3+
nOH pứ với Al3+ = 0,3 – 0,2x
(*) TH1 : Al3+ dư
=> 3nAl(OH)3 = nAl3+ => 0,18 = 0,3 – 0,2x
=> x = 0,6M
(*) TH2 : OH- hòa tan 1 phần Al(OH)3
=> nAl(OH)3 = 4nAl3+ - nOH
=> 0,06 = 4.0,08 – (0,3 – 0,2x)
=> x = 0,2 M
Đáp án B