
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

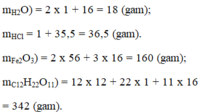

nh2o=18.6.1023=1,08.1025 mol
(18=1*2+16)
nhcl=36,5.6.1023=2,9.1025 mol
(36.5=35.5+1)
nfe2o3=160.6.1023=9,6.1025 mol
(160=56*2+16*3)
nc12h22o11=342.6.1023=2,052.1026 mol
(342=12*12+1*22+16*11)

Khối lượng của N phân tử các chất chính là khối lượng mol phân tử của các chất đã cho.
- Khối lượng mol phân tử H2O:
MH2O=1.2+16.1=18g
- Khối lượng mol phân tử HCl:
MHCl=1+35,5=36,5 g
- Khối lượng mol phân tử Fe2O3: MFe2O3=56.2+16.3=160g
- Khối lượng mol phân C12H22O11: MC12H22O11=12.12+1.22+16.11=342g

NH2O=1×2+16=18(g)
NHCl=1+35,5=36,5 (g)
NFe2O3= 56×2+16×3=160(g)
NC12H22O11= 12×12+22×1+16×11=342(g)
\(M_{H_2O}\) = 1.2 + 16 = 18 g
MHCl = 1 + 35,5 = 36, 5 g \(M_{Fe_2O_3}\) = 56 . 2 + 16 . 3 = 160 g \(M_{C_{12}H_{22}O_{11}}\) = 12 . 12 + 22 . 1 + 11 . 16 = 342 g
- Nguyên tử khối của Fe = 56 đvC
- Phân tử khối của C12H22O11 = 12.12+1.22+16.11 = 342 đvC
Cảm ơn bạn nha, bây h mình mới biết hai cái đó bằng nhau ^_^

lần sau chia nhỏ ra nha bạn
Bài 1:
Hướng dẫn: bài này e lấy khôi lượng mol từng chất nhân vs hệ số rồi chia cho khối lượng mol hợp chất nhân 100% nha e
VD:KOH
\(\%m_K=\frac{39}{56}.100\%=69,64\%\)
\(\%m_O=\frac{16}{56},100\%=28,57\%\)
\(\%m_H=100-69,64-28,57=1,79\%\)
Bài 2: Lập công thức hóa học của các hợp chất:
a)
\(\%Cu:\%S:\%O=40:20:40\)
\(\Rightarrow n_{Cu}:n_S:n_O=\frac{40}{64}:\frac{20}{32}:\frac{40}{16}=0,625:0,625:2,5\)
=\(1:1:4\)
\(PTK:160\)
\(\Rightarrow CTHH:CuSO4\)
b) B gồm 82,35% N và 17,65% H, biết khối lượng mol của B là 17.
c)
\(\%Na:\%S:\%O=32,39:22,53:45,48\)
\(\Rightarrow n_{Na}:n_S:n_O=\frac{32,39}{23}:\frac{22,52}{32}:\frac{45,08}{16}=1,4:0,7:2,8\)
=\(2:1:4\)
\(PTK:142\)
\(\Rightarrow CTHH:Na2SO4\)
Bài còn lại e làm tương tự nha
Bài 3: Hợp chất X có phân tử khối bằng 62 đvC. Trong hợp chất nguyên tố oxi chiếm 25% theo khối lượng còn lại là nguyên tố Na. Số nguyên tử của nguyên tố O và Na trong phân tử hợp chất là bao nhiêu?
\(\%Na:\%O=75:25\)
\(\Rightarrow n_{Na}:n_O=\frac{75}{23}:\frac{25}{16}=3,26:1,56\)
\(=2:1\)
\(PTK:62\Rightarrow CTHH:Na2O\)
Vậy số nguyên tử O là 1, số nguyên tử Na là 2
Bài 4:
\(\%K:\%Mn:\%O=26,68:34,82:40,51\)
\(n_K:n_{Mn}:m_O=\frac{26,68}{39}:\frac{34,81}{55}:\frac{40,51}{16}\)
\(=0,6:0,6:2,5=1:1:4\)
\(PTK=1,86.85=158\Rightarrow CTHH:KMnO4\)

bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g

Câu 10:
a) Fe2O3:
\(\%m_{Fe}=\dfrac{2.56}{2.56+3.16}.100=70\%\\ \Rightarrow\%m_O=100\%-70\%=30\%\)
b) CaCO3:
\(\%m_{Ca}=\dfrac{40}{40+12+3.16}.100=\dfrac{40}{100}.100=40\%\)
\(\%m_C=\dfrac{12}{40+12+3.16}.100=\dfrac{12}{100}.100=12\%\\ \Rightarrow\%m_O=100\%-\left(40\%+12\%\right)=48\%\)
c) HCl:
\(\%m_H=\dfrac{1}{1+35,5}.100=\dfrac{1}{36,5}.100\approx2,74\%\\ \Rightarrow\%m_{Cl}\approx100\%-2,74\%\approx97,26\%\)
2)Theo đề bài ta có: p+n+e=40=>2p+n=40(1)
n=p+12=>2p-n=12(2)
Từ (1) (2) ta có hệ
2p+n=40=>p=13
2p-n=12=>n=14
Vậy X là nitơ

\(CT:C_{12}H_{22}O_{11}\)
\(M=12\cdot12+22+11\cdot16=342\left(đvc\right)\)
\(\%C=\dfrac{12\cdot12}{342}\cdot100\%=42.1\%\)
\(\%H=\dfrac{22}{342}\cdot100\%=6.43\%\)
\(\%O=51.47\%\)

a;
PTK của đường là :
12.12+22.1+11.16=342(dvC)
b;
% C=\(\dfrac{12.12}{342}.100\%=42,1\%\)
% H =\(\dfrac{22}{342}=6,4\%\)
% O=\(\dfrac{16.11}{342}.100\%=54,46\%\)