
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a. PTHH:
Na2SO3 + H2SO4 ---> Na2SO4 + SO2 + H2O (1)
K2SO3 + H2SO4 ---> K2SO4 + SO2 + H2O (2)
Theo PT(1,2): \(n_{H_2SO_4}=n_{SO_2}=0,3\left(mol\right)\)
=> \(m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
b. Gọi x, y lần lượt là số mol của Na2SO3 và K2SO3
Theo PT(1,2):
=> x + y = 0,3
Theo đề, ta có: 126x + 158y = 44,2
=> x = 0,1, y = 0,2
Theo PT(1): \(n_{Na_2SO_4}=n_{Na_2SO_3}=0,1\left(mol\right)\)
=> \(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
Theo PT(2): \(n_{K_2SO_4}=n_{K_2SO_3}=0,2\left(mol\right)\)
=> \(m_{K_2SO_4}=0,2.164=34,8\left(g\right)\)
=> \(m_{sau.phản.ứng}=34,8+14,2=49\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{0,3.98}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
=> \(m_{dd_{H_2SO_4}}=147\left(g\right)\)
Ta có: \(m_{dd_{sau.phản.ứng}}=147+44,2=191,2\left(g\right)\)
=> \(C_{\%_{dd_{sau.phản.úng}}}=\dfrac{49}{191,2}.100\%=25,63\%\)
c. Đổi 500ml = 0,5 lít
=> \(n_{Ba\left(OH\right)_2}=1.0,5=0,5\left(mol\right)\)
Ta có: \(T=\dfrac{n_{SO_2}}{n_{Ba\left(OH\right)_2}}=\dfrac{0,3}{0,5}=0,6< 1\)
Vậy PTHH là: \(SO_2+Ba\left(OH\right)_2--->BaSO_3+H_2O\) (Ba(OH)2 dư.)
Theo PT: \(n_{BaSO_3}=n_{SO_2}=0,3\left(mol\right)\)
=> \(m_{BaSO_3}=0,3.217=65,1\left(g\right)\)
\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Na_2SO_3+H_2SO_4\rightarrow Na_2SO_4+H_2O+SO_2\)
\(x\) \(x\)
\(K_2SO_3+H_2SO_4\rightarrow K_2SO_3+H_2O+SO_2\)
\(y\) \(y\)
Ta có: \(\left\{{}\begin{matrix}126x+158y=44,2\\x+y=0,3\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
a)\(\Rightarrow\Sigma n_{H_2SO_4}=0,1+0,2=0,3mol\)
\(\Rightarrow m_{H_2SO_4}=0,3\cdot98=29,4\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{29,4}{20}\cdot100=147\left(g\right)\)
b)



Bài 1:
Ta có : 1 mol muối RCO3 (có khối lượng = R + 60n) chuyển thành 1 mol RCln (có khối lượng = R + 71n)
=> khối lượng tăng = 71n – 60n = 11n gam
=> Khi chuyển 1 mol gốc CO3 thành 2 mol gốc Cl và tạo ra 1 mol CO2 thì khối lượng tăng 11 gam
a) Ta có công thức tính nhanh sau : \(m_{muốiclorua}=n_{muốicacbonat}+11.n_{CO_2}\)
=> \(n_{CO_2}=\dfrac{11,1-10}{11}=0,1\left(mol\right)\)
=> \(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
b) \(MCO_3+2HCl\rightarrow MCl_2+CO_2+H_2O\)
\(n_{HCl}=2n_{CO_2}=0,2\left(mol\right)\)
=> \(m_{ddHCl}=\dfrac{0,2.36,5}{3,65\%}=200\left(g\right)\)
c) \(m_{ddsaupu}=10+200-0,1.44=205,6\left(g\right)\)
\(C\%_{muối}=\dfrac{11,1}{205,6}.100=5,4\%\)
d) \(n_{MCO_3}=n_{MCl_2}\)
=> \(\dfrac{10}{M+60}=\dfrac{11,1}{M+71}\)
=> \(M=40\left(Ca\right)\)

a. PTHH: CuO + H2SO4 ---> CuSO4 + H2O
b. Ta có: \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{CuO}=0,1\left(mol\right)\)
=> \(m_{H_2SO_4}=0,1.98=9,8\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{9,8}{m_{dd_{H_2SO_4}}}.100\%=4,9\%\)
=> \(m_{dd_{H_2SO_4}}=200\left(g\right)\)
c. Ta có: \(m_{dd_{CuSO_4}}=200+8=208\left(g\right)\)
Theo PT: \(n_{CuSO_4}=n_{CuO}=0,1\left(mol\right)\)
=> \(m_{CuSO_4}=0,1.160=16\left(g\right)\)
=> \(C_{\%_{CuSO_4}}=\dfrac{16}{208}.100\%=7,69\%\)

a) Khối lượng giảm là khối lượng kim loại đã phản ứng
Hỗn hợp + H2SO4 loãng dư
Giả sử A phản ứng hết, B không phản ứng
\(A+H_2SO_4\rightarrow ASO_{\text{ 4 }}+H_2\)
\(n_{H_2}=n_A=0,1\left(mol\right)\)
=> \(M_A=\dfrac{6,5}{0,1}=65\left(Zn\right)\)
\(m_B=6,66-6,5=0,16\left(mol\right)\)
B + H2SO4 đặc nóng
\(B\rightarrow B^{2+}+2e\) \(S^{+6}+2e\rightarrow S^{+4}\)
Bảo toàn e: \(n_B.2=n_{SO_2}.2\Rightarrow n_B=n_{SO_2}=\dfrac{0,16}{64}=0,0025\left(mol\right)\)
=>\(M_B=\dfrac{0,16}{0,0025}=64\left(Cu\right)\)
Vậy A là Zn, B là Cu (thỏa mãn )
b\(\%m_{Zn}=\dfrac{6,5}{6,66}.100=97,6\%;\%m_{Cu}=2,4\%\)


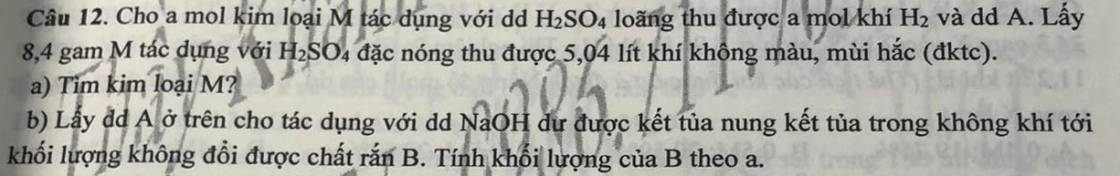 gấp lắm rùi ạa
gấp lắm rùi ạa giúp với ạa
giúp với ạa






