Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Tham khảo
mCaCO3= 80%. m(đá vôi)= 80%. 500=400(g)
-> nCaCO3= mCaCO3/M(CaCO3)=400/100=4(mol)
PTHH: CaCO3 -to-> CaO + CO2
Ta có: nCaO(LT)= nCaCO3= 4(mol)
=> mCaO(LT)=56.4=224(g)
Đặt x là số mol CaCO3 (p.ứ) -> Số mol CaO tạo thành là x (mol) (x>0)
=> Khối lượng rắn tạo thành là:
(400 - 100x) + 56x + 100= 78%. 500
<=>x=2,5(mol)
Vì KL tỉ lệ thuận số mol:
=> H(p.ứ)= (2,5/4).100= 62,5%

Coi mhh ban đầu = 100g
⇒%mAl2O3 = 1/8 * 100% = 12,5%
PTHH
CaCO3 ➜ CaO + CO2
MgCO3 ➜ MgO + CO2
Gọi số mol của CaCO3 và MgCO3 lần lượt là x và y, ta có:
100x + 84y = (100 - 1/8 * 100) = 87,5 (1)
lại có:
(100 - mCO2) / 100 = [100 - 44(x+y)] / 100 = 6/10
⇒x + y = 0.91 (2)
Giải (1) và (2) ta được: x = 0,69125; y = 0,21875
%mCaCO3 = [(0,69125 * 100) / 100] * 100% = 69,125%
%mMgCO3 = 100% - 12,5% - 69,125% = 18,375%

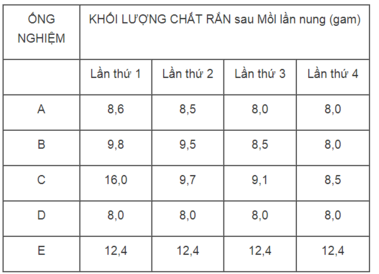
1. Ống nghiệm E (khối lượng CuCO 3 không thay đổi).
2. Ống nghiệm C, vì khác với các kết quả của những ống nghiệm A, B, D.
3. Sau lần nụng thứ 3 thì toàn lượng CuCO 3 đã bị phân huỷ hết thành CuO.
4. Ống nghiệm D.

Ta có: mCaCO3 = 500.80% = 400 (g)
m chất rắn = 400.78% = 312 (g)
Theo ĐLBT KL, có: mCO2 = 400 - 312 = 88 (g)
\(\Rightarrow n_{CO_2}=\dfrac{88}{44}=2\left(mol\right)\)
PT: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
_____2_____________2 (mol)
\(\Rightarrow m_{CaCO_3\left(pư\right)}=2.100=200\left(g\right)\)
Bạn tham khảo nhé!

PTHH:
\(2KMnO_4-^{t^o}\rightarrow K_2MnO_4+MnO_2+O_2\)
\(KClO_3-^{t^o}\rightarrow KCl+\dfrac{3}{2}O_2\)
2KCl + MnO2 + 2H2SO4 \(-^{t^o}\rightarrow\) K2SO4 + MnSO4 + Cl2 + 2H2O
4KCl + K2MnO4 + 4H2SO4 \(-^{t^o}\rightarrow\) 3K2SO4 + MnSO4 + 2Cl2 + 4H2O

mCaCO3= 80%. m(đá vôi)= 80%. 500=400(g)
-> nCaCO3= mCaCO3/M(CaCO3)=400/100=4(mol)
PTHH: CaCO3 -to-> CaO + CO2
Ta có: nCaO(LT)= nCaCO3= 4(mol)
=> mCaO(LT)=56.4=224(g)
Đặt x là số mol CaCO3 (p.ứ) -> Số mol CaO tạo thành là x (mol) (x>0)
=> Khối lượng rắn tạo thành là:
(400 - 100x) + 56x + 100= 78%. 500
<=>x=2,5(mol)
Vì KL tỉ lệ thuận số mol:
=> H(p.ứ)= (2,5/4).100= 62,5%

Như vậy khi phản ứng Cu xảy ra hoàn toàn thì khối lượng tăng lên 1/4
Theo đề bài, sau phản ứng khối lượng chất rắng
Cu tăng lên 1/6 khối lượng bạn đầu => Cu chưa bị oxi hóa hết thu được CuO và Cu còn dư
Giả sử thí nghiệm với 128 Cu. Theo đề, g oxi phản ứng:
128/6 = 21,333 g
Theo PTHH của phản ứng số g Cu đã phản ứng với số g oxi và số g CuO được tạo thành:
128.32 . 21,333 = 85,332 g ; mCuO = 160/32 21,333 = 106,665 g
Số g Cu còn lại :
128 - 85,332 = 42,668 g
%Cu = \(\frac{42,668}{149,333}100=28,57\%\) => %CuO = 71,43%