
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 8 :
a) \(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
\(n_{Al}=\dfrac{54}{27}=2\left(mol\right)\)
b) \(V_{CO_2}=0,15.22,4=3,36\left(l\right)\)
\(V_{N_2}=0,3.22,4=6,72\left(l\right)\)
c) \(n_{hh}=n_{CO_2}+n_{H_2}=\dfrac{0,22}{44}+\dfrac{0,02}{2}=0,015\left(mol\right)\)
\(V_{hh}=0,015.22,4=0,336\left(l\right)\)
Câu 9
a) \(m_N=0,3.14=4.2\left(g\right)\)
\(m_{Cl}=0,4.35,5=14,2\left(g\right)\)
\(m_O=5.16=80\left(g\right)\)
b) \(m_{N_2}=0,2.28=5,6\left(h\right)\)
\(m_{Cl_2}=0,3.71=21,3\left(g\right)\)
\(m_{O_2}=4.32=128\left(g\right)\)
c) \(m_{Fe}=0,12.56=6,72\left(g\right)\)
\(m_{Cu}=3,15.64=201,6\left(g\right)\)
\(m_{H_2SO_4}=0,85.98=83,3\left(g\right)\)
\(m_{CuSO_4}=0,52.160=83,2\left(g\right)\)

Bài 6 :
$a) M = X + 16.3 = M_{Br} = 80 \Rightarrow X = 32$
$b) M = X + 4.1 = M_{S} = 32 \Rightarrow X = 28$
$c) M = 2X + 32 = 2M_{S} = 2.32 = 64 \Rightarrow X = 16$
Bài 6 :
Theo đề ta có : \(\dfrac{M_{X2S3}}{M_{CuSO4}}\)
\(\dfrac{M_{X2S3}}{160}\)
⇒ MX2S3 = 160 - 10 = 150 (dvc)
Có : MX2S3 = 150 (dvc)
2.MX + 3.MS = 150
⇒ 2.MX + 3.32 = 150
⇒ 2.MX + 96 = 150
⇒ 2.MX = 150 - 96 = 54
⇒ MX = \(\dfrac{54}{2}=27\) (dvc)
Vậy nguyên tố x là nhôm
kí hiệu : Al
Chúc bạn học tốt

Câu 4:
a. Gọi CTHH là: \(\overset{\left(III\right)}{Fe_x}\overset{\left(II\right)}{O_y}\)
Ta có: III . x = II . y
=> \(\dfrac{x}{y}=\dfrac{II}{III}=\dfrac{2}{3}\)
=> \(\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\)
Vậy CTHH là: Fe2O3
b. Gọi CTHH là: \(\overset{\left(II\right)}{Cu_a}\overset{\left(II\right)}{\left(SO_4\right)_b}\)
Ta có: II . a = II . b
=> \(\dfrac{a}{b}=\dfrac{II}{II}=\dfrac{2}{2}=\dfrac{1}{1}\)
=> \(\left\{{}\begin{matrix}a=1\\y=1\end{matrix}\right.\)
Vậy CTHH là: CuSO4
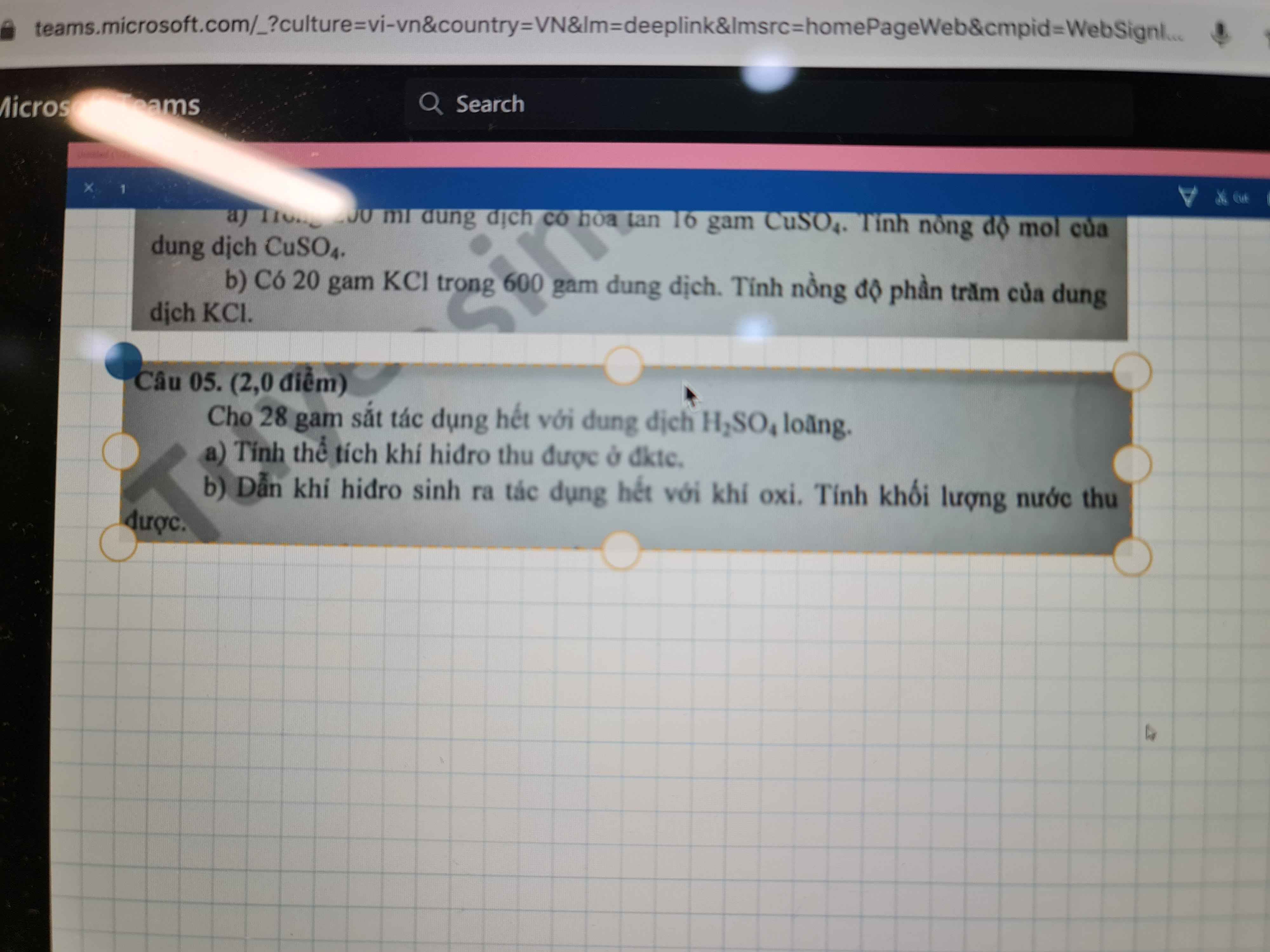
Câu 5:
Gọi CTHH của hợp chất A là: M2SO4
Theo đề, ta có: \(PTK_{M_2SO_4}=142\left(đvC\right)\)
Mà: \(PTK_{M_2SO_4}=NTK_M.2+32+16.4=142\left(đvC\right)\)
=> NTKM = 23(đvC)
Vậy M là natri (Na)

n Fe=0,5 mol
Fe+H2sO4->FeSO4+H2
0,5----------------------------0,5
=>VH2=0,5.22,4=11,2l
b) 2H2+O2-to>2H2O
0,5-------------------0,5
=>m H2O=0,5.18=9g
a. \(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
PTHH : Fe + H2SO4 ( loãng ) -> FeSO4 + H2
0,5 0,5
\(V_{H_2}=0,5.22,4=11,2\left(l\right)\)
b. PTHH : 2H2 + O2 -> 2H2O
0,5 0,5
\(m_{H_2O}=0,5.18=9\left(g\right)\)



 giúp mình với mình chỉ cần 2 câu 8 với câu 9 thôi nha
giúp mình với mình chỉ cần 2 câu 8 với câu 9 thôi nha 



 giải giúp mình câu 5 với ạ
giải giúp mình câu 5 với ạ 
Bài 5:
n\(Na_2ZnO_2\) = \(\dfrac{8,58}{143}=0,06mol\)
n\(Mg_3\left(PO_4\right)_2\) =\(\dfrac{7,86}{262}=0,03mol\)
\(n_{CuSO_4}=\dfrac{7,42}{160}=0,046375\approx0,046mol\)
\(n_{CO_2}=\dfrac{26,88}{22,4}=1,2mol\)
\(n_{NO}=\dfrac{20,16}{22,4}=0,9mol\)
\(n_{NO_2}=\dfrac{16,8}{22,4}=0,75mol\)
\(n_{CuSO_4}=\dfrac{1,2.10^{23}}{6.10^{23}}=0,2mol\)
\(n_{Fe}=\dfrac{4,8.10^{23}}{6.10^{23}}=0,8mol\)
n\(Na_3PO_4\) = \(\dfrac{15,3.10^{23}}{6.10^{23}}=2,55mol\)