Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,05___________0,05___0,05
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
0,045_____________ 0,09________
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,05______________0,05____________
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
0,09_______________ 0,09_________________
\(4Fe\left(OH\right)_2+O_2+H_2O\rightarrow4Fe\left(OH\right)_3\)
0,05 _______________________0,05
\(n_{H2}=\frac{11,2}{22,4}=0,05\left(mol\right)\)
\(\rightarrow m_{Fe2O3}=10-0,05.56=7,2\left(g\right)\)
\(n_{Fe2O3}=\frac{7,2}{160}=0,045\left(mol\right)\)
\(\rightarrow n_{Fe\left(OH\right)3}=0,05+0,09=0,14\left(mol\right)\)
\(2Fe\left(OH\right)_3\rightarrow Fe_2O_3+3H_2O\)
0,14 ________0,07_________
\(\rightarrow m_{Fe2O3}=0,07.160=11,2\left(g\right)\)
HH { Fe , Fe2O3) qua phản ứng với HCl và NaOH. Rồi lấy kết tủa nung nóng trong không khí dc lượng chất rắn không đổi chính là Fe2O3 ( 2Fe(OH)3 -> Fe2O3 + H2O)
Vậy ta thấy hh ban đầu là { Fe , Fe2O3} và hh sau cùng là Fe2O3 đều là hợp chất của Fe. Áp dụng định luật bảo toàn nguyên tố ta sẽ có:
Số mol Fe trong hh ban đầu = số mol Fe ở hh sau cùng.
**Muốn tình tổng số mol Fe ở hh ban đầu cần số mol Fe và nFe2O3:
Biết Fe + 2HCL -> FeCl2 + H2
.......0,05<------------------1.12/22,4 = 0,05 mol
=>mFe trong hh đầu là : 0,05 *56 = 2,8 (g)
=>nFe2O3 trong hh đầu là (10 - 2,8)/160 = 0,045 mol
=> nFe có trong Fe2O3 của hh ban đầu là : 0,045 *2 = 0,09 (mol)
Vậy tổng số mol của Fe trong hh ban đầu là : 0,09 + 0,05 = 0,14 mol
Và 0,14 mol đó cũng chính là n Fe trong hh thu sau cùng. Nhưng đề bài cần mình tính m Fe2O3 thu sau cùng nên ta cần biết n Fe2O3
Biết nFe2O3 = 1/2 * nFe (trong Fe2O3) = 0,14 / 2 = 0,07 (mol)
=> Khối lượng chất rắn Y là : 0,07 * 160 =11,2 (g)

HH { Fe , Fe2O3) qua phản ứng với HCl và NaOH. Rồi lấy kết tủa nung nóng trong không khí dc lượng chất rắn không đổi chính là Fe2O3 ( 2Fe(OH)3 -> Fe2O3 + H2O)
Vậy ta thấy hh ban đầu là { Fe , Fe2O3} và hh sau cùng là Fe2O3 đều là hợp chất của Fe. Áp dụng định luật bảo toàn nguyên tố ta sẽ có:
Số mol Fe trong hh ban đầu = số mol Fe ở hh sau cùng.
**Muốn tình tổng số mol Fe ở hh ban đầu cần số mol Fe và nFe2O3:
Biết Fe + 2HCL -> FeCl2 + H2
.......0,05<------------------1.12/22,4 = 0,05 mol
=>mFe trong hh đầu là : 0,05 *56 = 2,8 (g)
=>nFe2O3 trong hh đầu là (10 - 2,8)/160 = 0,045 mol
=> nFe có trong Fe2O3 của hh ban đầu là : 0,045 *2 = 0,09 (mol)
Vậy tổng số mol của Fe trong hh ban đầu là : 0,09 + 0,05 = 0,14 mol
Và 0,14 mol đó cũng chính là n Fe trong hh thu sau cùng. Nhưng đề bài cần mình tính m Fe2O3 thu sau cùng nên ta cần biết n Fe2O3
Biết nFe2O3 = 1/2 * nFe (trong Fe2O3) = 0,14 / 2 = 0,07 (mol)
=> Khối lượng chất rắn Y là : 0,07 * 160 =11,2 (g)

Fe+2HCl->FeCl2+H2
Fe2O3+6HCl->2FeCl3+3H2O
nH2=1,12/22,4=0,05(mol)
nFe=nH2=0,05(mol)
mFe2O3=10-0,05x56=7,2 g
nFe2O3=7,2/160=0,045(mol)
FeCl2+2NaOH->Fe(OH)2+2NaCl
0,05 ------------------ 0,05
FeCl3+3NaOH->Fe(OH)3+3NaCl
0,045 ----------------- 0,045
4Fe(OH)2+O2+2H2O->4Fe(OH)3
0,05---------------------------0,05
nFe(OH)3=0,05+0,045=0,095(mol)
2Fe(OH)3to->Fe2O3+3H2O
0,095 ----------- 0,0475
mFe2O3=0,0475x160=7,6 g
tại sao số mol của fecl3 khi tác dụng với naoh lại là 0,045 mol???

Đáp án B
nSO2 = 1,7 (mol)
Chất rắn Z là Fe2O3, nFe2O3 = 0,4 (mol)
2Febđ → Fe2O3
0,8 ← 0,4 (mol)
Ta có: mX = 1,7 ×64 – 48=60,8 (gam)
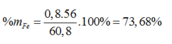

Đáp án D
A chứa : FeO,FeO,Fe2O3,Fe3O4
B chứa : FeSO4,Fe2(SO4)3
C : Fe(OH)2,Fe(OH)3
D : Fe2O3(vì nung ngoài không khí nên sẽ không còn FeO)

Đầu tiên, chúng ta sẽ viết các phương trình phản ứng cho mỗi bước của quá trình.
Bước 1: Phản ứng giữa hỗn hợp Fe và Al với dung dịch HCl: HCl (dung dịch) + Fe (kim loại) → FeCl2 (dung dịch) + H2 (khí)
2HCl + Fe → FeCl2 + H2
Bước 2: Phản ứng giữi dung dịch X với NaOH tạo kết tủa: X (dung dịch) + 2NaOH → 2NaX (dung dịch) + H2O (lỏng) + Al(OH)3 (kết tủa)
Bước 3: Nung kết tủa Al(OH)3 trong không khí: 2Al(OH)3 → Al2O3 + 3H2O
Bây giờ, chúng ta sẽ tính toán m và a.
Bước 1: Tính lượng H2 thoát ra.
Trước hết, chúng ta cần biết lượng mol của Fe trong hỗn hợp. Công thức của FeCl2 là Fe2+ (một cation sẽ tạo ra 1 mol H2 khi phản ứng với HCl). Vì vậy, số mol của Fe là bằng số mol H2.
Khối lượng mol của H2 là 2 g/mol, vì vậy số mol H2:
n(H2) = 5.6 l / 22.4 l/mol (ở điều kiện tiêu chuẩn) = 0.25 mol
Do đó, số mol Fe = 0.25 mol.
Khối lượng mol của Fe là 55.85 g/mol, vậy khối lượng của Fe là:
m(Fe) = 0.25 mol × 55.85 g/mol = 13.96 g
Bước 2: Tính lượng kết tủa Al(OH)3.
Al(OH)3 có khối lượng mol là 78 g/mol, và theo phương trình phản ứng ta thấy rằng mỗi mol Al(OH)3 tạo ra một mol kết tủa. Vì vậy, số mol Al(OH)3 tạo ra là bằng số mol NaOH đã sử dụng.
Số mol NaOH đã sử dụng được tính theo số mol H2O được tạo ra khi NaOH phản ứng. Một mol NaOH phản ứng với một mol H2O.
n(Al(OH)3) = n(NaOH) = n(H2O) = 0.25 mol
Khối lượng của Al(OH)3:
m(Al(OH)3) = 0.25 mol × 78 g/mol = 19.5 g
Bước 3: Nung kết tủa Al2O3 trong không khí.
Khối lượng của Al2O3 không thay đổi sau quá trình nung. Vì vậy, a = 19.5 g (cùng với m(Al(OH)3)).
Tóm lại:
m = 19.5 g (kết tủa Al(OH)3)a = 19.5 g (sau khi nung thành Al2O3)Các PTHH :
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
\(4Fe\left(OH\right)_2+O_2\xrightarrow[]{t^o}2Fe_2O_3+4H_2O\)
\(2Al\left(OH\right)_3\xrightarrow[]{t^o}Al_2O_3+3H_2O\)
Kết tủa thu được gồm Fe(OH)2 và Al(OH)3
Đặt : \(n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(\Rightarrow56a+27b=8,3g\left(1\right)\)
\(Bte:2n_{Fe}+3n_{Al}=2n_{H2}=2a+3b=2.\dfrac{5,6}{22,4}=\left(2\right)\)
Từ(1),(2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1=n_{Fe\left(OH\right)2}\\b=0,1=n_{Al\left(OH\right)3}\end{matrix}\right.\)
\(\Rightarrow m_{kết.tủa}=m_{Fe\left(OH\right)2}+m_{Al\left(OH\right)3}=0,1.90+0,1.78=16,8\left(g\right)\)
\(Bt\left(Al\right):n_{Al}=n_{Al2O3}=0,1\left(mol\right)\)
\(Bt\left(Fe\right):n_{Fe}=n_{Fe2O3}=0,1\left(mol\right)\)
\(\Rightarrow m_{Chất.rắn}=0,1.160+0,1.102=26,2\left(g\right)\)
Chúc bạn học tốt