Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số mol của natri oxit
nNa2O = \(\dfrac{m_{Na2O}}{M_{Na2O}}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
Pt : Na2O + H2O→ 2NaOH\(|\)
1 1 2
0,1 0,2
Số mol của dung dịch natri hidroxit
nNaOH = \(\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
Nồng độ mol của dung dịch natri hidroxit
CMNaOH = \(\dfrac{0,2}{2}=0,1\left(M\right)\)
⇒ Chọn câu : C
Chúc bạn học tốt
nNa2O = mNa2O : MNa2O = 6,2 : (23 . 2 + 16) = 0,1 mol
PTHH: Na2O + H2O → 2NaOH
Tỉ lệ 1 2
Phản ứng 0,1 ? mol
Từ PTHH => nNaOH = 2 nNa2O = 0,2 mol
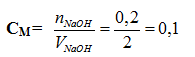
bạn coi thử

\(n_{Na_2O}=\dfrac{6,2}{62}=0,1mol\\ Na_2O+H_2O\rightarrow2NaOH\\ n_{NaOH}=0,1.2=0,2mol\\ C_{M_X}=C_{M_{NaOH}}=\dfrac{0,2}{2}=0,1M\)
\(n_{Na_2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
PT: \(Na_2O+H_2O\rightarrow2NaOH\)
Theo PT: \(n_{NaOH}=2n_{Na_2O}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{0,2}{2}=0,1\left(m\right)\)

Sửa đề: 9,2 gam Na
\(a,n_{Na_2O}=\dfrac{9,2}{23}=0,4\left(mol\right)\)
PTHH: \(Na_2O+H_2O\rightarrow2NaOH\)
0,4------------------>0,8
\(\rightarrow C_{M\left(NaOH\right)}=\dfrac{0,8}{0,5}=1,6M\)
\(b,n_{K_2O}=\dfrac{37,6}{94}=0,4\left(mol\right)\)
PTHH: \(K_2O+H_2O\rightarrow2KOH\)
0,4----------------->0,8
\(\rightarrow C\%_{KOH}=\dfrac{0,8.56}{362,4+37,6}.100\%=11,2\%\)

\(a,C_{M\left(NaOH\right)}=\dfrac{0,3}{0,5}=0,6M\\ b,n_{NaOH}=\dfrac{24}{40}=0,6\left(mol\right)\\ C_{M\left(NaOH\right)}=\dfrac{0,6}{0,4}=1,5M\)

a)
\(n_{H_2}=\dfrac{0,336}{22,4}=0,015\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,03<------------0,03<----0,015
=> \(\%m_{Na}=\dfrac{0,03.23}{1,31}.100\%=52,67\%\)
=> \(\%m_{Na_2O}=100\%-52,67\%=47,33\%\)
b)
\(n_{Na_2O}=\dfrac{1,31.47,33\%}{62}=0,01\left(mol\right)\)
PTHH: Na2O + H2O --> 2NaOH
0,01----------->0,02
=> nNaOH = 0,03 + 0,02 = 0,05 (mol)
mdd sau pư = 1,31 + 18,72 - 0,015.2 = 20 (g)
=> \(C\%_{dd.NaOH}=\dfrac{0,05.40}{20}.100\%=10\%\)
\(V_{dd.NaOH}=\dfrac{20}{1,2}=\dfrac{50}{3}\left(ml\right)=\dfrac{1}{60}\left(l\right)\)
\(C_{M\left(dd.NaOH\right)}=\dfrac{0,05}{\dfrac{1}{60}}=3M\)

\(n_{Na_2O}=\dfrac{12,4}{62}=0,2\left(mol\right)\\ Na_2O+H_2O\rightarrow2NaOH\\ n_{NaOH}=0,2.2=0,4\left(mol\right)\\ C_{MddNaOH}=\dfrac{0,4}{0,4}=1\left(M\right)\)

Câu 1 :
a) n Na2O = 3,1/62 = 0,05(mol)
$Na_2O + H_2O \to 2NaOH$
Theo PTHH : n NaOH = 2n Na2O = 0,1(mol)
=> CM NaOH = 0,1/2 = 0,05M
Câu 2 :
Coi n KOH = 1(mol)
=> V dd KOH = 1/2 = 0,5(lít) = 500(ml)
=> mdd KOH = D.V = 500.1,43 = 715(gam)
=> C% KOH = 1.56/715 .100% = 7,83%
1. Ta có : \(n_{Na_2O}=\dfrac{m}{M}=0,05mol\)
\(PTHH:Na_2O+H_2O\rightarrow2NaOH\)
Theo PTHH: \(n_{NaOH}=2n_{Na_2O}=0,1mol\)
\(\Rightarrow C_{MNaOH}=\dfrac{n}{V}=0,05M\)
2. - Gọi số lít KOH là a lít
\(\Rightarrow m_{dd}=D.V=1430a\left(g\right)\)
Mà \(n_{KOH}=C_M.V=2amol\)
\(\Rightarrow m_{KOH}=n.M=112a\left(g\right)\)
\(\Rightarrow C\%=\dfrac{m}{m_{dd}}.100\%=\dfrac{112a}{1430a}.100\%=~7,83\%\)
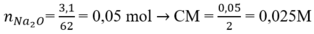
\(n_{Na_2O}=\dfrac{6.2}{62}=0.1\left(mol\right)\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(0.1...........................0.2\)
\(C_{M_{NaOH}}=\dfrac{0.2}{1}=0.2\left(M\right)\)