Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì Cu không phản ứng với HCl
=> mCu = 2,54 (g)
=> mMg và Al = 9,14 - 2,54 = 6,6 (g)
nH2 = \(\dfrac{7,84}{22,4}\)= 0,35 (mol)
Gọi x và lần lượt là số mol của Mg và Al
Mg + 2HCl ----> MgCl2 + H2
x x x (mol)
2Al + 6HCl ----> 2AlCl3 + 3H2
y y \(\dfrac{3}{2}\)y (mol)
Theo đề ra, ta có:
24x + 27y = 6,6
x + \(\dfrac{3}{2}\)y = 0,35
=> x = 0,05
y = 0,2
=> mMg = 0,05.24 = 1,2 (g)
=> mAl = 0,2.27 = 5,4 (g)
=> %Cu = \(\dfrac{2,54.100\%}{9,14}\)= 28%
=> %Mg = \(\dfrac{1,2.100\%}{9,14}\)= 13%
=> %Al = 100 - 28 - 13 = 59%
mMgCl2 = 0,05.95 = 4,75 (g)
mAlCl3 = 0,2.133,5 = 26,7 (g)
=> m = 4,75 + 26,7 = 31,45 (g)

a)Gọi x,y lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu (x,y>0)
Sau phản ứng hỗn hợp muối khan gồm: \(\left\{{}\begin{matrix}AlCl_3:x\left(mol\right)\\FeCl_2:y\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}27x+56y=13,9\\133,5x+127y=38\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,0896\\y\approx0,205\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,0896\cdot27\cdot100\%}{13,9}\approx17,4\%\\\%m_{Fe}=\dfrac{0,205\cdot56\cdot100\%}{13,9}\approx82,6\%\end{matrix}\right.\)
Theo Bảo toàn nguyên tố Cl, H ta có:\(n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{3n_{AlCl_3}+2n_{FeCl_2}}{2}\\ =\dfrac{3\cdot0,0896+2\cdot0,205}{2}=0,3394mol\\ \Rightarrow V_{H_2}=0,3394\cdot22,4\approx7,6l\)

E có 1 chút nhầm lẫn ở câu cuối
Mg + 2HCl ‐> MgCl + H ﴾1﴿ 2Al + 6HCl ‐> 2AlCl + 3H ﴾2﴿ Fe + 2HCl ‐> FeCl + H ﴾3﴿
Theo bài ra ta có : H2 = = 0,4 ﴾mol﴿ Thep ptpu ﴾1﴿﴾2﴿﴾3﴿ ta thấy HCl = H2 = 0,4 .2 = 0,8 ﴾mol﴿ => HCl = 0,8 .36,5 = 26,8 ﴾g﴿ Ap dụng định luật bảo toàn khối lượng : m hỗn hợpMg ,Al,Fe + HCl= m muối MgCl , ALCL , FeCl + H ﴾=﴿ 15+26,8 =m+0,4.2 ﴾=﴿ 41,8 =m +0,8 => m=41,8 -0,8=41﴾g﴿Mg + 2HCl -> MgCl2 + H2 (1)
2Al + 6HCl -> 2AlCl3 + 3H2 (2)
Fe + 2HCl -> FeCl2 + H2 (3)
Theo bài ra ta có : nH2 =\(\frac{8,69}{22,4}\) = 0,4 (mol)
Thep ptpu (1)(2)(3) ta thấy
nHCl = 2nH2 = 0,4 .2 = 0,8 (mol)
=> m HCl = 0,8 .36,5 = 26,8 (g)
Ap dụng định luật bảo toàn khối lượng : m hỗn hợpMg ,Al,Fe +m HCl= m muối MgCl2 , ALCL3, FeCl2 +mH2
(=) 15+26,8 =m+0,4.2
(=) 41,8 =m +0,8
=> m=41,8 =0,8=41(g)

a) Sửa đề: dd H2SO4 9,8%
Ta có: \(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\) \(\Rightarrow m_{H_2}=0,35\cdot2=0,7\left(g\right)\)
Bảo toàn nguyên tố: \(n_{H_2SO_4}=n_{H_2}=0,35\left(mol\right)\) \(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,35\cdot98}{9,8\%}=350\left(g\right)\)
\(\Rightarrow m_{dd}=m_{KL}+m_{H_2SO_4}-m_{H_2}=361,6\left(g\right)\)
b) Tương tự câu a
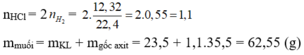
Đáp án A
Chất rắn Y là Cu không phản ứng
nHCl =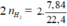 = 2.0,35 = 0,7
= 2.0,35 = 0,7
mmuối = mKL + mgốc axit = (9,14 – 2,54) + 0,7.35,5 = 31,45(g)