Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A.
Do NaOH dư nên có phản ứng
![]()
2NaOH + SO2 → Na2SO3 + H2O
0,3 0,3 (mol)
Gọi hóa trị của M là x
Bảo toàn e ta có nM.x = nSO2.2 => nM = 0,6/x
MM = 32x, Với x = 2, M = 64 (Cu)

Đáp án D.
nSO2 = 0,55 => ne = 0,55.2 = 1,1 (mol)
mmuối = mKL + Mgốc axit. ne/2
= 14,6 + 96. 1,1/2 = 67,4 g

Quy đổi hỗn hợp kim loại thành R, có soh là +n
\(n_R=\dfrac{17,1}{M_R}\left(mol\right)\)
R0 - ne --> R+n
\(\dfrac{17,1}{M_R}\)->\(\dfrac{17,1n}{M_R}\)
S+6 + 2e --> S+4
1<---0,5
Bảo toàn e: \(\dfrac{17,1n}{M_R}=1\Rightarrow M_R=17,1n\)
Muối thu được có CTHH là R2(SO4)n
\(n_{R_2\left(SO_4\right)_n}=\dfrac{17,1}{2.M_R}\left(mol\right)\)
=> \(m_{R_2\left(SO_4\right)_n}=\dfrac{17,1}{2.M_R}\left(2.M_R+96n\right)=17,1+\dfrac{820,8n}{M_R}=65,1\left(g\right)\)

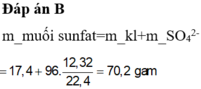
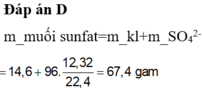

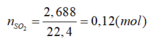
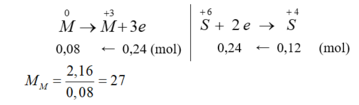
Đáp án D
Khi hấp thụ SO2 hết vào dung dịch NaOH thì có thể xảy ra các phản ứng sau:
SO2 + 2NaOH → Na2SO3 + H2O
SO2 + NaOH → NaHSO3
Gọi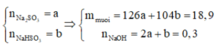
Khi đó
Gọi n là hóa trị của M.
Áp dụng định luật bảo toàn mol electron, ta có:
Mặt khác
Là Cu