Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

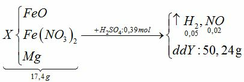
Vì Mg có tính khử rất mạnh nên trong Y có thể có muối (NH4)2SO4
BTNT N: 2nFe(NO3)2 = nNO + nNH4 => 2y = 0,02 + nNH4 => nNH4 = 2y – 0,02
BTNT H: 2nH2SO4 = 2nH2 + 4nNH4 + 2nH2O => 2 . 0,39 = 2 . 0,05 + 4 (2y – 0,02) + 2nH2O
=> nH2O = 0,38 – 4y
BTNT O: nFeO + 6nFe(NO3)2 = nNO + nH2O
=> x + 6y = 0,02 + 0,38 – 4y => x + 10y = 0,4
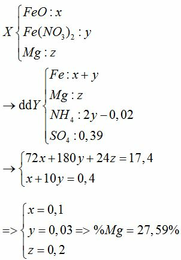

PTHH: Fe + H2SO4 → FeSO4 + H2 ↑
Số mol của H2 là: 0,224 : 22,4 = 0,01(mol)
Số mol của Fe là: 0,01 mol
Khối lượng của Fe là: 0,01 . 56 = 0,56 gam
- Trong 2,88 gam hỗn hợp X có 0,56 gam Fe => Trong 5,76 gam Hỗn hợp X sẽ có 1,12 gam Fe.
Khối lượng FeO và Fe2O3 trong 5,76 gam hỗn hợp X là: 5,76 - 1,12 = 4,64 (gam)
PTHH: FeO + H2 → Fe + H2O
Fe2O3 + 3H2 → 2Fe + 3H2O
Gọi số mol của FeO là a , Số mol của Fe2O3 là b
=> Số mol của H2O ở pt (1) là a, Số mol của H2O ở pt (2) là 3b
Ta có hệ phương trình:
- 72a + 160b = 4,64
- 18a + 54b = 1,44
=> a = 0,02 ; b = 0,02
Khối lượng của FeO trong 5,76 gam hỗn hợp X là:
72a = 72 . 0,02 = 1,44 (gam)
Khối lượng của Fe2O3 trong 5,76 gam hỗn hợp X là:
160b = 160 . 0,02 = 3,2 (gam)
% FeO trong hh X là: (1,44 : 5,76).100% = 25%
% Fe2O3 trong hh X là: (3,2:5,76).100% = 55,56%
% Fe trong hh X là: (1,12 : 5,76 ) .100% = 19,44%

a có:
nNO=0,05(mol) ;nH2=0,4(mol) và mZ=2,3(g)
Muối sunfat trug hòa có thể gồm FeSO4 , Fe2(SO4)3 , (NH4)2SO4, K2SO4, Al2(SO4)3
áp dụng định luật bảo toàn khối lượng
66,2 + 3,1.136=466,6+0,45.469 + mH2O → mH2O=18,9(g) → nH2O=1,05(mol)
Đặt nNH4+=x(mol). Ta có 3,1=4x+2.1,05 + 2.0,4 → x= 0,05(mol)
Vậy nNO3=0,05+0,05=0,1(mol) → nFe(NO3)2=0,05(mol)
Bảo toàn nguyên tố O ta được 4a + 0,05.6 =1,05 + 0,05
a=0,2(mol) (Với a=nFe3O4)
=>mAl =66,2-0,2.232-180.0,05 =10,8(g)
%Al = 16,1%.

\(a)Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ b)n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\\ n_{Fe}=n_{H_2}=0,1mol\\ m_{Fe}=0,1.56=5,6g\\ m_{Fe_2O_3}=21,6-5,6=16g\\ c)n_{Fe_2O_3}=\dfrac{16}{160}=0,1mol\\ n_{H_2SO_4}=0,1+0,1.3=0,4mol\\ C_{M_{H_2SO_4}}=\dfrac{0,4}{0,5}=0,8M\)

Qui đổi hh X về Fe, Cu, Mg, Zn và S
Gọi số mol e cho của hh kim loại là x và số mol của S là y
Ta có m kim loại = 10,42 – 32y

m kết tủa lớn nhất = mM(OH)n + mBaSO4
mM(OH)n = m kim loại + mOH- = 10,42 – 32y + 17x
n BaSO4 = nSO42- =x/2 => mBaSO4 =x/2 .233
=> m kết tủa = 10,42 – 32y + 17x + x/2.233 = 43,96 (2)
Từ (1) và (2) => x = 0,28 và y = 0,12
=> m = 10,42 – 32 . 0,12 + . 96 = 20,02

\(3Cu+8H^++2NO_3^-\rightarrow2NO+4H_2O+3Cu^{2+}\)
3z---->8z----->2z
\(2H^++O^{2-}\rightarrow H_2O\)
2y<---y
\(Cu+2Fe^{3+}\rightarrow Cu^{2+}+2Fe^{2+}\)
x---->2x
+ Hỗn hợp ban đầu: \(\left\{{}\begin{matrix}Fe^{3+}:2x\\O:y\\Cu:x+3z\\NO_3:2z\end{matrix}\right.\)
\(\Sigma n_{Fe}=2x=\dfrac{2z}{3}+\dfrac{2y}{3}\Leftrightarrow3x=y+z\left(1\right)\)
\(\Sigma n_{H^+\left(H_2SO_4\right)}=2y+8z=0,42.2=0,84\left(2\right)\)
\(m=37,06=56.2x+16y+64\left(x+3z\right)+62.2z\left(3\right)\)
Từ (1), (2), (3), giải được \(\left\{{}\begin{matrix}x=0,065\\y=0,12\\z=0,075\end{matrix}\right.\)
Số mol mỗi chất trong X: \(\left\{{}\begin{matrix}n_{Fe\left(NO_3\right)_3}=\dfrac{2z}{3}=\dfrac{2.0,075}{3}=0,05\left(mol\right)\\n_{Fe_2O_3}=\dfrac{y}{3}=\dfrac{0,12}{3}=0,04\left(mol\right)\\n_{Cu}=x+3z=0,065+3.0,075=0,29\left(mol\right)\end{matrix}\right.\)