

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



khi cho Fe vào HCl tạo Fe2+
áp dụng định luật bảo toàn e ta có:
Fe => Fe2+ + 2e 2H+ +2e => H2
nFe = 0,05 mol => mFe=2,8 g => mFe2O3 =7,2g => nFe2O3=0,045 mol
nói chung khi nung kết tủa trong không khí đều tạo Fe2O3 => m (chất rắn)= 7,6 g

Đáp án B
Có:
![]()
= 0,24 +3.0,1 = 0,54 mol
![]() = 0,22 mol
= 0,22 mol
· mkết tủa = ![]()
Lượng kết tủa thu được lớn nhất khi S O 2 - 4 kết tủa hoàn toàn và khối lượng Al ( O H ) 3 là lớn nhất.
![]()
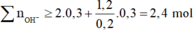
![]()
![]()
=> Al(OH)3 bị tan ra
![]() => Al(OH)3 tan hết
=> Al(OH)3 tan hết
![]()
= 97,1 (g)
Gần nhất với giá trị 97,08

Đáp án C
X tan trong 0,3 mol H2SO4 và 1,1 mol HCl thu được dung dịch chứa Y chứa:
Fe2+ 0,24 mol, Mg2+ 0,2 mol, Al3+ 0,2 mol, H+ dư 0,22 mol, SO42-0,3 mol và Cl- 1,1 mol.
Nhỏ từ từ hỗn hợp chứa Ba(OH)2 0,2M và NaOH 1,2M đến khối lượng kết tủa lớn nhất.
Gọi thể tích dung dịch thêm vào là V, dung dịch này chứa Ba2+0,2V, Na+ 1,2V và OH- 1,6V.
Để kết tủa hidroxit lớn nhất thì cần số mol OH-=0,24.2+0,2.2+0,2.3+0,22=1,7 mol.
Để kết tủa BaSO4 lớn nhất thì số mol Ba2+ là 0,3 mol tương đương với thêm vào 2,4 mol OH-.
Vậy có sự hòa tan Al(OH)3 tuy nhiên kết tủa vẫn tăng do có tạo thành BaSO4 bù vào.
Vậy kết tủa thu được là Fe(OH)2 0,24 mol Mg(OH)2 0,2 mol và BaSO4 0,3 mol.
Nung kết tủa trong không khí đến khối lượng không đổi được Fe2O3 0,12 mol, MgO 0,2 mol và BaSO4 0,3 mol.
=> m = 97,1 gam

Tăng giảm khối lượng ta có mO/MgO = 28 – 20 = 8 gam.
Bảo toàn nguyên tố Mg ta có nMg = nMgO = 8 ÷ 16 = 0,5 mol.
⇒ nNO2 = 2nMg = 1 mol Û VNO2 = 22,4 lít
Đáp án D

Chọn A.
Dung dịch Y gồm Cu2+ (0,12 mol), Mg2+ (0,1 mol), Al3+ (0,1 mol), H+(dư) (0,11 mol), SO42- (0,15 mol) và Cl- (0,55 mol).
Khi cho dung dịch hỗn hợp Ba(OH)2 0,1M và NaOH 0,6M vào Y đến khi thu được khối lượng kết tủa lớn nhất thì ta xét hai trường hợp sau:



Đáp án C
28g chất rắn gồm MgO và Fe2O3=> mO trong MgO = 28 – 20 = 8g => nMg = mO = 0,5
Bảo toàn ne=> nNO2 = 2nMg = 1 => V = 22,4