Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D.
![]()
⇒ số Ctrong X = số Ctrong Y = 1,5 ÷ 0,5 = 3 ⇒ X là C3H8O.
số Htrung bình = 1,4 × 2 ÷ 0,5 = 5,6 ⇒ số Htrong Y < 5,6 ⇒ số Htrong Y bằng 2 hoặc 4.
Đặt nX = x mol; nY = y mol (x < y) ||⇒ nM = x + y = 0,5 mol.
s TH1: Y là C3H2O2. Ta có: ![]() 4x + 2y = 1,4 mol ⇒ x = 0,3 mol; y = 0,2 mol → loại.
4x + 2y = 1,4 mol ⇒ x = 0,3 mol; y = 0,2 mol → loại.
s TH2: Y là C3H4O2. Ta có: ![]() 4x + 2y = 1,4 mol ⇒ x = 0,2 mol; y = 0,3 mol (thỏa mãn.!)
4x + 2y = 1,4 mol ⇒ x = 0,2 mol; y = 0,3 mol (thỏa mãn.!)
⇒ Y là CH2=CH-COOH ⇒ este là CH2=CH-COOC3H7.⇒ meste = 0,2 × 0,8 × 114 = 18,24 gam.

Đáp án : D
Số C = nCO2/nhh = 3. Vậy ancol là C3H7OH -> 4H2O.
Vì nH2O < nCO2 => axit không no
Axit có 3C có 2 trường hợp :
+) CH2=CH-COOH -> 2H2O : x + y = 0,5 và 4x + 2y = 1,4
=> x = 0,2 và y = 0,3 (nhận)
+) CH≡C-COOH -> 1H2O : x + y = 0,5 và 4x + y = 1,4
=> x = 0,3 và y = 0,2 ( Loại : nY < nX)
Este là CH2=CH-COOC3H7 với mCH2=CHCOOC3H7 = 0,2.0,8.144 = 18,24g

Ta có số mol CO2= 1,5 mol.
Theo bài ra, vì axit và ancol có c ng số nguyên tử C
=> số nguyên tử C trong mỗi chất là 1,5: 0,5=3.
=> ancol C3H7OH. axit là C3H6O2 hoặc C3H4O2.
Giải hệ 2 phương trình 2 ẩn với số mol và số mol H2O thu
đc
=> axit là CH2=CH-COOH.
n ancol=0,2. naxit=0,3 => m este=0,2. 114. 0,75 = 17,1 (g)
Chọn A

Đáp án : A
n C O 2 = 0,15 mol
=> Số C mỗi chất trong M = 3
=> ancol là C3H7OH : x mol
n H 2 O = 0,14 mol => Số H trung bình = 5,6
+) TH1 : Số H trong axit = 2
=> C3H2O2 : CH≡C-COOH : y mol
=> nM = x + y = 0,05 ; nH = 8x + 2y = 0,14.2
=> x = 0,03 ; y = 0,02 mol ( Loại vì naxit phải lớn hơn nancol)
+) TH2 : Số H trong axit = 4
=> C3H4O2 : CH2=CH-COOH : y mol
=> x = 0,02 ; y = 0,03 mol
=> n C H 2 = n C H C O O C 3 H 7 = 0,02.80% = 0,016 mol
=> meste = 1,824g
(Do naxit > nancol => Tính H theo axit)

Đáp án B
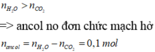
Áp dụng định luật bảo toàn khối lượng cho phản ứng đốt cháy ta có:
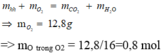
Áp dụng định luật bảo toàn nguyên tố oxi:
nO trong ancol + nO trong axit + nO trong O2
= nO trong CO2 + nO trong H2O
=> nO trong axit = 2.0,3 + 0,4 - 0,1 - 0,8 = 0,1 mol
=> naxit= 0,05 mol
Gọi m, n lần lượt là số ntử C của ancol, axit m ≠ n
=> 0,1m + 0,05n = 0,3
=> m =1, n=4
=> CTPT: CH3OH, C3H7COOH
=> CT este C3H7COOCH3
=> phản ứng este hóa, ancol dư 0,05 mol, axit hết
=> meste lí thuyết = 005.102 = 5,1 g
=> meste thực tế = 5,1.80% = 4,08g

Chọn đáp án D
7,6(g) X + ?O2 → 0,3 mol CO2 + 0,4 mol H2O. Bảo toàn khối lượng:
||⇒ mO2 = 0,3 × 44 + 0,4 × 18 - 7,6 = 12,8(g) ⇒ nO2 = 0,4 mol. Bảo toàn nguyên tố Oxi:
nO/X = 0,3 × 2 + 0,4 – 0,4 × 2 = 0,2 mol. Do nCO2 < nH2O ⇒ ancol no, đơn chức, mạch hở.
Ta có: nCO2 – nH2O = (k – 1).nHCHC (với k là độ bất bão hòa của HCHC).
► Áp dụng: nancol = ∑nH2O - ∑nCO2 = 0,1 mol ⇒ naxit = (0,2 - 0,1) ÷ 2 = 0,05 mol.
Đặt số C của axit và ancol là a và b ⇒ 0,1a + 0,05b = 0,3 → a ≠ b a , b ≥ 1 a = 1 và b = 4
⇒ X gồm HCOOH và C4H9OH. Do naxit < nancol ⇒ hiệu suất tính theo axit.
► Este là HCOOC4H9 với số mol 0,04 ⇒ m = 0,04 × 102 = 4,08(g) ⇒ chọn D

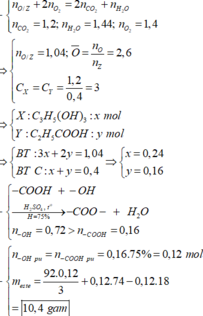
Chọn đáp án D