Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
E gồm 2 este không no dạng CnH2n – 2O2 (n là giá trị trung bình, n > 5)
và một este no dạng CmH2mO2 (m là giá trị nguyên, m ≥ 3).
(ở đây cần chú ý ancol tạo este là C2H5OH nên n > 5 và m ≥ 3 là vì thế).
• giải đốt 5 , 1 g a m E + O 2 → t 0 0 , 23 m o l C O 2 + 0 , 21 m o l H 2 O
mE = mC + mH + mO
⇒ mO trong E = 1,92 gam
⇒ n X = 1 2 n O t r o n g E = 0 , 06 m o l
Tương quan đốt: n C n H 2 n – 2 O 2 = ∑ n C O 2 – ∑ n H 2 O = 0 , 02 m o l ⇒ n C m H 2 m O 2 = 0 , 04 m o l
có Ctrung bình = 0,23 ÷ 0,06 ≈ 3,833
→ este no là HCOOC2H5.
⇒ C t r u n g b ì n h 2 e s t e k h ô n g n o = ( 0 , 23 – 0 , 04 × 3 ) ÷ 0 , 02 = 5 , 5
⇒ đọc ra được có 0,01 mol C2H3COOC2H5 (Y) và 0,01 mol C3H5COOC2H5 (Z).
Yêu cầu: % m e s t e Y t r o n g E = 0 , 01 × 100 ÷ 5 , 1 × 100 % ≈ 19 , 61 %

Đáp án : A
Thứ nhất, có 0,04 mol H2 nên số mol ancol = 0,08
Khối lượng ancol là 2.48 + 0,04.2 = 2.56 => 3,56/0,08 = 32 = CH3OH
Ta có thể suy ra thêm:
Trong 5,88g (0,08mol) hỗn hợp có 0,08 mol O (vì có có 2O trong tất cả các este đơn chất)
số mol H2O = 0,22 nên số mol H = 0,44
Bảo toàn khối lượng được số mol C = 0,24
C trung bình = 3 nên nhất định phải có 1 chất là C2H4O2, chất đồng đẳng là C3H6O3, chất còn lại là este của C4H6O2 và methanol nên là C5H8O2.
lập hệ 3 phương trình:
x + y + z = 0,08
(2.14+32)x + (3.14 + 32)y + (5.14+ 32)z = 5,88
2x + 3y + 5z = 0.24
x = 0,04 ; y = 0,02 ; z = 0,02
=> %mC5H8O2 = 34,01%

Đáp án : C
Thứ nhất, có 0,04 mol H2 nên số mol ancol = 0,08
Khối lượng ancol là 2.48 + 0,04.2 = 2.56 => 3,56/0,08 = 32 = CH3OH
Ta có thể suy ra thêm:
Trong 5,88g (0,08mol) hỗn hợp có 0,08 mol O (vì có có 2O trong tất cả các este đơn chất)
số mol H2O = 0,22 nên số mol H = 0,44
Bảo toàn khối lượng được số mol C = 0,24
C trung bình = 3 nên nhất định phải có 1 chất là C2H4O2, chất đồng đẳng là C3H6O3, chất còn lại là este của C4H6O2 và methanol nên là C5H8O2.
lập hệ 3 phương trình:
x + y + z = 0,08
(2.14+32)x + (3.14 + 32)y + (5.14+ 32)z = 5,88
2x + 3y + 5z = 0.24
x = 0,04 ; y = 0,02 ; z = 0,02
=> %mC5H8O2 = 34,01%

Chọn C.
n Y = 2 n H 2 = 0 , 08 m Y - m H 2 = 2 , 48 ⇒ m Y = 2 , 56 M Y = 32
Y là CH3OH.
n X = n Y = 0 , 08 M X = 5 , 88 0 , 08 = 73 , 5 X g ồ m H C O O C H 3 ; C H 3 C O O C H 3 C m H 2 m - 1 C O O C H 3

Đáp án B
- Xét Ancol + Na dư → H2. Có: nH2 = 0,896: 22,4 = 0,04 mol
=> nancol = 2nH2 = 0,08 mol
mbình tăng + mH2 = mancol => mancol = 2,48 + 0,04.2 = 2,56g
=> Mancol = 2,56: 0,08 = 32g => CH3OH
=> X gồm 2 este no dạng CnH2n+1COOCH3 và 1 este không no dạng CmH2m-1COOCH3
(Với n là giá trị trung bình, n > 0 ; m là số nguyên, m ≥ 2)
- Xét phản ứng cháy 5,88g X. nX = 0,08 mol
Có: nH2O = 3,96: 18 = 0,22 mol
nO(X) = 2nX = 2nCOO(X) = 0,16 mol và mX = mC + mH + mO
=> nC = 0,24 mol = nCO2
Tương quan ta có: neste không no = nCO2 – nH2O = 0,02 mol => n2 este no = 0,08 – 0,02 = 0,06 mol
Ctrung bình = 0,24: 0,08 = 3 => 2 este no là HCOOCH3 và CH3COOCH3
(Vì este không no phải có ít nhất 4C => số C trung bình của 2 este no < 3)
=> số C trung bình của 2 cacbon no nằm trong khoảng (2 ; 3)
- Bảo toàn C: nC(X) = Ctb no.nno + Ckhông no.nkhông no
=> (0,24 – 3.0,06) < 0,02.Ckhông no < (0,24 – 2.0,06)
=> 3 < Ckhông no < 6
Vì nếu C = 4 => CH2=CHCOOCH3 => không có đồng phân hình học => Loại
Vậy Ckhông no = 5 => CH3-CH=CH-COOCH3
=> %mEste không no = 0,02.100: 5,88 = 34,01%



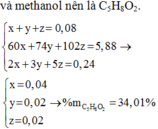


Chọn đáp án C
X gồm 2 este no dạng CnH2nO2 (n là giá trị trung bình, n > 2)
và một este không no dạng CmH2m – 2O2 (m là giá trị nguyên, m ≥ 4).
• giải đốt 5 , 6 g a m X + O 2 → t 0 0 , 22 m o l C O 2 + 0 , 2 m o l H 2 O
mX = mC + mH + mO
⇒ mO trong X = 2,56 gam
⇒ n X = 1 2 n O t r o n g X = 0 , 08 m o l
Tương quan đốt: n C m H 2 m – 2 O 2 = ∑ n C O 2 – ∑ n H 2 O = 0 , 02 m o l ⇒ n C n H 2 n O 2 = 0 , 06 m o l
có Ctrung bình = 0,22 ÷ 0,08 = 2,75
→ 2 este no là HCOOCH3 và CH2COOCH3.
chặn khoảng giá trị có: ( 0 , 22 – 0 , 06 × 3 ) ÷ 0 , 02 = 2 < m < ( 0 , 22 – 0 , 06 × 2 ) ÷ 0 , 02 < 5
kết hợp điều kiện ban đầu: 4 ≤ m < 5
⇒ este không no là C2H3COOCH3.
Yêu cầu: % m e s t e k h ô n g n o t r o n g X = 0 , 02 × 86 ÷ 5 , 6 × 100 % ≈ 30 , 71 %