Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
X: HOCH2CH2OH (a mol), C2H5OH (b mol), C3H7OH (c mol), C6H14 (a mol)
Vì số mol etilenglicol bằng số mol hexan nên đặt công thức chung cho 2 chất là C4H9OH (a mol)
X + Na dư:
n H 2 = 1 2 . ( a + b + c ) = 0 , 4032 22 , 4 = 0 , 018 m o l ⇒ a + b + c = 0 , 036 m o l
Đặt công thức chung cho X là CnH2n+1OH
C n H 2 n + 2 O + 3 n 2 O 2 → t o n C O 2 + ( n + 1 ) H 2 O
n O 2 = 3 n 2 . ( a + b + c ) = 4 , 1664 22 , 4 = 0 , 186 m o l ⇒ 3 n 2 . 0 , 036 = 0 , 186 ⇒ n = 31 9
⇒ m = 0 , 036 . 596 9 = 2 , 384 g a m

Chọn A
Hỗn hợp X gồm 3 chất là ancol metylic, etylen glicol và glixerol, nhưng lại chỉ có một giả thiết nên coi hỗn hợp X chỉ gồm 1 chất là ancol metylic.
Theo bảo toàn nguyên tố C và bảo toàn nguyên tố H trong nhóm -OH, ta có
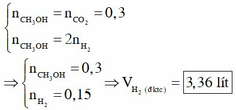

Đáp án là B
Fructozo + H2 → sobitol : C6H8(OH)6 (X)
(Y) : CH3OH , C3H5(OH)3
Nhận thấy , trong X và Y , đều có
nOH- = nC =0,25 (mol)
Khi Y tác dụng với Na dư , ta có :
n H 2 = 1 2 nOH- = 0, 125 (mol)
=> V = 2,8(l)

Đáp án là D
Phản ứng đốt cháy muối:
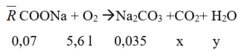
BTKL:
mmuối + mO2 = mNa2CO3 + mCO2 + mH2O
? 7,06 + 5,6.32/22,4 = 0,035.106 + 44x + 18y (1)
BT oxy:
2.0,07 + 2.0,25 = 3.0,035 + 2x + y (2)
Từ (1) và (2)
? x = 0,215 mol và y = 0,105 mol
Vậy trong 2 muối:

? 1 muối có 3C và 1 muối có 4C
Dùng phương pháp đường chéo sẽ có: n( muối 3C) = 0,03 mol và n(muối 4C) = 0,04 mol
Tính được:
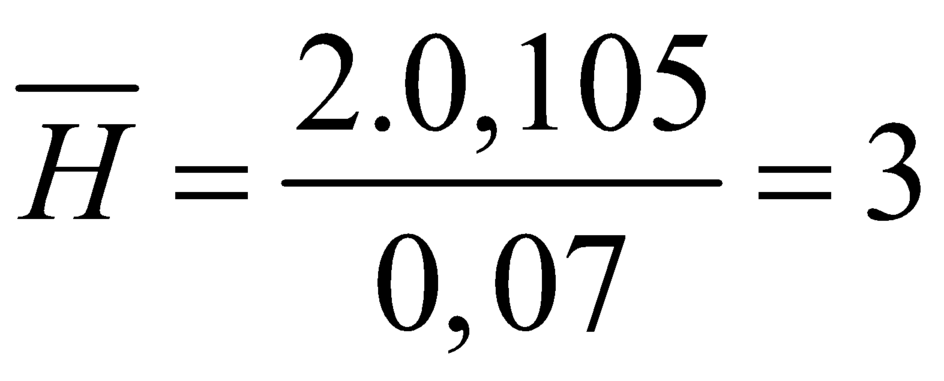
Mà số H trong muối thì lẻ nên cả 2 muối trong phân tử đều có 3H
Nên công thức của 2 este có thể viết là: C2H3COOCnH2n+1 và C3H3COOCnH2n+1 ( vì thủy phân trong NaOH tạo ra 1 ancol no đơn chức )
PT đốt cháy etse:
C2H3COOCnH2n+1 + O2 ? (3+n)CO2 + (n+2)H2O
C3H3COOCnH2n+1 + O2 ? (4+n)CO2 + (n+2)H2O
Theo phương trình:
nCO2 = 0,03.(3 + n) + 0,04.(4 + n) = 0,25 + 0,07n
nH2O = 0,03.(2 + n) + 0,04.(2 + n) = 0,14 + 0,07n
toàn Oxy: 0,07.2 + 2.0,46 = 2.( 0,25 + 0,07n) + 0,14 + 0,07n
? n = 2
Vậy CT của 2 este là: C2H3COOC2H5 và C3H3COOC2H5
? % m C3H3COOC2H5 = 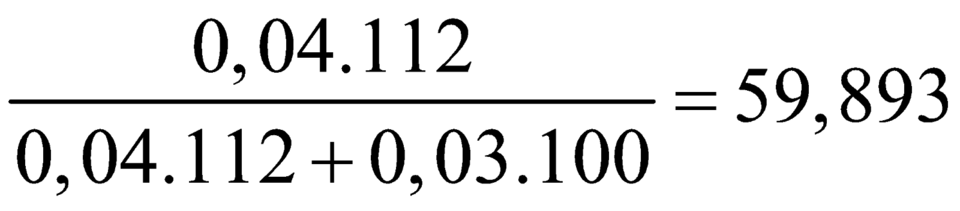 %
%

hai ancol no là đồng đẳng kế tiếp nhau gọi chung là A:CnH2n+2Oz (n lớn hơn 1)
một ancol không no có một nối đôi C=C hai chức B:CmH2mO2 (m lớn hơn 2)
đốt cháy X tạo
nCO2=n.số mol A+m. mol B
nH2O=(n+1)mol A +m. mol B
nH2O-nCO2=mol A=0,15
A tác dụng Na thực chất là
(OH)z + zNa --> (ONa)z +z/2H2
0,15 0,075
Mol H2 còn lại là 0,085-0,075=0,01
B tác dụng Na thực chất là
(OH)2+2Na --> (ONa)2 +H2
0,01 0,01
Bảo toàn cac bon 0,15 n + 0,01 m= 0,2
Suy ra m=3,n=17/15 suy ra X có CH3OH, C2H5OH,C3H4(OH)2
Hoặc m=4, n=16/15 suy ra X có CH3OH,C2H5OH, C4H6(OH)2
……

Chọn đáp án D
Phần 1 Y: n 1 / 2 Y = 2 n H 2 = 2. 0 , 84 22 , 4 = 0 , 075 m o l
Phần 2 Y: Đốt cháy thu được 0,2 mol CO2
m gam X tác dụng vừa đủ với 0,25 mol H2
Đặt a, b lần lượt là số mol của A và B trong X, k là độ bội liên kết của B
⇒ a + b = 0 , 075.2 = 0 , 15 m o l n H 2 = a + k b = 0 , 25 m o l ⇒ b = 0 , 1 k + 1
Có b > a ⇒ b > 0,075 ⇒ 0 , 15 > 0 , 1 k − 1 > 0 , 075 ⇒ 1 , 67 < k < 2 , 33 ⇒ k = 2
⇒ a = 0 , 05 b = 0 , 1 ⇒ n C O 2 = 1 2 . ( C A .0 , 05 + C B .0 , 1 ) = 0 , 2 ⇒ C A + 2 C B = 8 ⇒ C A = 2 C B = 3
⇒ A : C H 3 C H O B : C H 2 = C H C H O ⇒ % m B = 56.0 , 1 56.0 , 1 + 44.0 , 05 .100 % = 71 , 79 %
gần với giá trị 70,25% nhất.

Đáp án B
nO2 đốt X = 0,46
nO2 đốt Y = 0,25
=> nO2 đốt Z = 0,46 - 0,25 = 0,21
Z no, đơn chức, mạch hở nên nCO2 = 0,21/1,5 = 0,14
Nếu X mạch hở thì nX = nZ = nNaOH = 0,07
=> Z là C2H5OH
Bảo toàn khối lượng
mX = mY + mZ - mNaOH = 7,48
Đặt a, b là số mol CO2 và H2O
=> 2a + b = 0,07 . 2 + 0,46 . 2 và 44a + 18b = 7,48 + 0,46 . 32
=> a = 0,39 và b = 0,28
=> Số C = 5,57 => C5 (0,03 mol) và C6 (0,04 mol)
Các muối gồm C2HxCOONa (0,03) và C3HyCOONa (0,04)
=> mY = 0,03(x + 91 ) + 0,04(y +103) = 7,06
=> 3x + 4y = 21 —> X = y = 3 là nghiệm duy nhất Xgồm:
C2H3COOC2H5 (0,03 mol)
C3H3COOC2H5 (0,04 mol)
=> % = 59,893%

Đáp án C
n C O 2 = 0,2 mol; n H 2 = 0,05 mol → n - O H a n c o l = 0,1 mol → n C t r o n g a n c o l ≥ 0,1 mol;
n N a O H = n O t r o n g Z = 0,1 → n C m u ố i ≥ 0,1 mol.
n C t r o n g E = n C t r o n g a n c o l + n C m u ố i = n C O 2 = 0,2 mol
→ n C t r o n g a n c o l = 0,1 mol; n C m u ố i = 0,1 mol.
→ Ancol có số C = số O; muối có số C = số Na. Vậy ancol là C H 3 OH (0,1 mol); các muối là HCOONa a mol và C O O N a 2 b mol
Bảo toàn Na có: a + 2b = n N a O H = 0,1 mol (1).
m m u ố i = 6,76 gam → 68a + 134b = 6,76 gam (2)
Từ (1) và (2) có a = 0,06 và b = 0,02.
X là HCOOC H 3 0,06 mol và Y là C O O C H 3 2 0,02 mol.
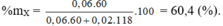
Chọn B
45%.