Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D.
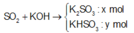
Ta có hệ phương trình
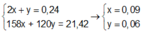
![]()
Gọi hóa trị của kim loại M là n
Áp dụng định luật bảo toàn electron ta có
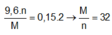
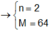

Thí nghiệm 1 :
\(n_{Mg} = a(mol) ; n_{Fe} = b(mol) \\ \Rightarrow 24a + 56b = 15,6(1)\\ Mg + H_2SO_4 \to MgSO_4 + H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{H_2} =a + b = 0,3(2)\\ (1)(2) \Rightarrow a = 0,0375 ; b = 0,2625\)
Thí nghiệm 2 : Vì khối lượng thí nghiệm 1 bằng 3 lần khối lượng thí nghiệm 2 nên ở thì nghiệm 2 : \(n_{Mg} = \dfrac{0,0375}{3}=0,0125(mol)\\ n_{Fe} = \dfrac{0,2625}{3} = 0,0875(mol)\\ \text{Bảo toàn electron : }\\ n_{SO_2} = \dfrac{0,0125.2 + 0,0875.3}{2} = 0,14375(mol)\\ m_X - m_{SO_2} = 5,2 - 0,14375.64 = -4\)
Vậy khối lượng dung dịch Z giảm 4 gam so với H2SO4 ban đầu.

Đáp án B
Phản ứng nhiệt phân:
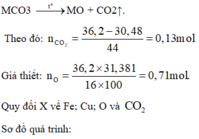
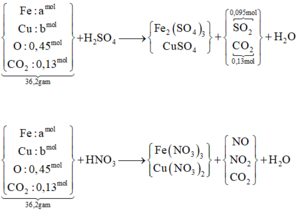
Gọi số mol các chất như sơ đồ, ta có: 56a + 64b + 0,45 ×16 + 0,13 ×44 = 36,2 gam
« Xét phản ứng với H2SO4: bảo toàn electron ta có: 3a + 2b = 0,45 × 2+ 0,095 × 2
Giải hệ các phương trình trên, ta được a = 0,29 mol và b = 0,11 mol.
« Xét phản ứng với HNO3, gọi số mol NO, NO2 lần lượt là x, y mol
Bảo toàn electron ta có 3 x + 2 y = 2 n SO 2 = 2 × 0,095 = 0,19 mol
Khối lượng hỗn hợp khí: 30x +46y + 0,13 × 44 = 42,25 × (x + y + 0,13)
Giải hệ phương trình, ta có: x = 0,04 mol; y = 0,07 mol
Bảo toàn nguyên tố N, ta có số mol HNO3 bằng 0,29 × 3 + 0,11 × 2 + 0,04 + 0,07 = 1,2 mol
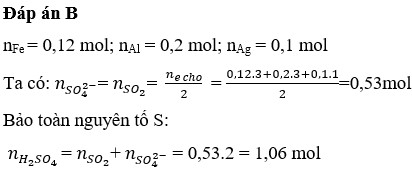
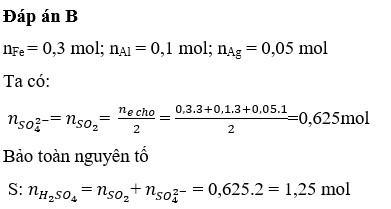
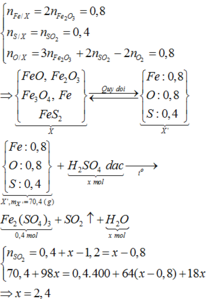
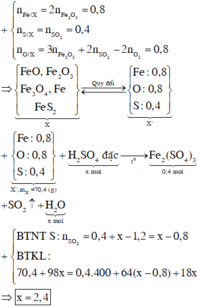
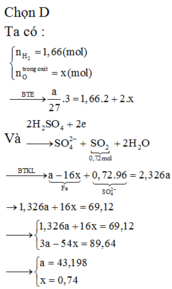

Đáp án C:
Dung dịch H2SO4đậm đặc vừa là chất oxi hóa vừa là môi trường.
Gọi a là số oxi hóa của S trong X.
có
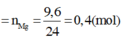
Áp dụng định luật bảo toàn mol electron, ta có:
Do đó X là H2S