Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bước 1: Viết cấu hình electron của N (Z = 7) và H (Z = 1)
N (Z = 7): 1s22s22p3
H (Z = 1): 1s1
Bước 2: Biểu diễn sự hình thành các cặp electron chung cho NH3
H có 1e ở lớp electron ngoài cùng, N có 5e ở lớp electron ngoài cùng.
⟹ Mỗi nguyên tử góp chung 1e để đạt cấu hình khí hiếm bền vững.
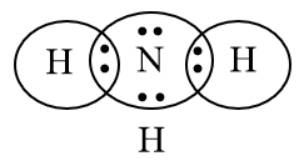
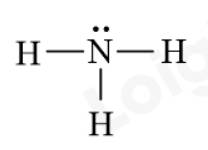
Bước 3: Công thức Lewis của NH3

- Trong phân tử phosphorus trichloride gồm 2 nguyên tố: P và Cl
+ Nguyên tử P có 5 electron ở lớp ngoài cùng => Góp chung 3 electron độc thân để hình thành 3 liên kết cộng hóa trị
+ Nguyên tử Cl có 7 electron ở lớp ngoài cùng => 3 nguyên tử Cl, mỗi nguyên tử góp chung 1 electron độc thân để hình thành 3 liên kết cộng hóa trị với P.
=> Khi đó, quanh P và Cl đều có 8 electron như khí hiếm Argon.
- Công thức Lewis của phân tử:


Chọn C
Cấu hình electron của N (z = 7): 1s22s22p3, có 5 electron ở lớp ngoài cùng.
Trong phân tử N2, để đạt cấu hình electron của khí hiếm gần nhất (Ne), mỗi nguyên tử nitơ phải góp chung 3 electron.

- Từ công thức electron của CO2:
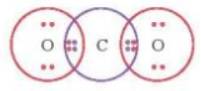
⟹ Mỗi nguyên tử O có 2 cặp electron dùng chung với nguyên tử C.
- Viết công thức Lewis của CO2: O = C = O

Chọn C
Cấu hình electron nguyên tử N: N có 5electr 1 s 2 2 s 2 2 p 3 . on lớp ngoài cùng, do đó khi hình thành liên kết trong phân tử N 2 , mỗi nguyên tử N sẽ góp chung 3 electron.
- Cấu hình electron của N (Z = 7): 1s22s22p3
- Để đạt cấu hình của khí hiếm gần nhất, mỗi nguyên tử N đều cần thêm 3 electron. Vì vậy mỗi nguyên tử N cùng góp 3 electron để tạo nên 3 cặp electron chung cho 2 nguyên tử N.
⟹ Số cặp electron dùng chung là 3.
⟹ Công thức Lewis của N2: