Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Sử dụng đường chéo ta tính được phần trăm số nguyên tử H 1 và H 2 :
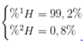
Thành phần % về khối lượng của 2H trong H2O là:
2 . 0 , 008 . 2 16 + 2 . 1 , 008 = 0 , 178 %

\(\%^1H=a;\%^2H=100\%-a\left(a>0\right)\\\overline{NTK}_H=1,008\\ \Leftrightarrow\dfrac{1.a+2.\left(100\%-a\right)}{100\%}=1,008\\ \Leftrightarrow a=99,2\%\\ \Rightarrow^1H=99,2\%;\%^2H=0,8\%\)
Số nguyên tử của đồng vị 2H có trong 9ml nước là:
\(\dfrac{9.1}{18}.6.10^{23}.\dfrac{2}{18}.0,8\%\approx2,667.10^{20}\left(nguyên.tử\right)\)

Gọi % đồng vị
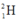
là a:
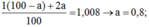

m của 1ml H2O: 1 gam
⇒ MH2O = 2. 1,008 + 16 = 18,016u
Khối lượng của 1 mol H2O là 18,016g.
Khối lượng của 1 mol H2O là 18,016g.
Số mol H2O =

mol
⇒ số mol nguyên tử H = 2.nH2O =
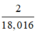
mol
1 mol nguyên tử chứa 6,022.1023 nguyên tử
⇒ Số nguyên tử H trong 1ml H2O =
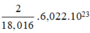
⇒ Số nguyên tử
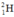

\(Đặt:\%^1H=a\\ \%^2H=100\%-a\\ Vì:\overline{NTK}_H=1,008\\ \Leftrightarrow\dfrac{1.a+2.\left(100\%-a\right)}{100\%}=1,008\\ \Leftrightarrow a=99,2\%\Rightarrow\%^1H=99,2\%;\%^2H=0,8\%\)
Số nguyên tử 2H có trong 1ml nước là:
\(0,8\%.\dfrac{1.1.2}{18}\approx8,889\%\)
Đáp án D
Gọi số mol của 2 đồng vị lần lượt là a và b