Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

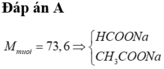
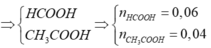
n Ag = 0 , 24 mol
Từ 4 đáp án, Y là ancol đơn chức
Nếu Y là CH3OH
![]()
Như vậy, 2 chất là HCOOCH3 và CH3COOH
Nếu Y không phải CH3OH
![]()

Đáp án C
● Cách 1: Tính toán theo phương trình phản ứng
Khối lượng hỗn hợp X tăng lên so với khối lượng ancol ban đầu là do lượng O trong CuO phản ứng đã chuyển vào H 2 O và CH 3 COOH .
Theo giả thiết, suy ra :
n H 2 = 0 , 0375 n CuO phản ứng = n O phản ứng
= (3,3 - 2,3):16 = 0,0625
Gọi số mol của ancol tham gia phản ứng là x, y và số mol ancol dư là z.
Phương trình phản ứng :
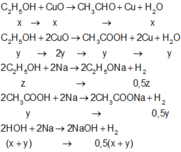
⇒ n C 2 H 5 OH bđ = x + y + z = 0 , 05 n H 2 = 0 , 5 y + 0 , 5 z + 0 , 5 x + 0 , 5 y = 0 , 0375 n CuO pư = x + 2 y = 0 , 0625 ⇒ x = 0 , 0125 ; y = 0 , 025 ; z = 0 , 0125 H = 0 , 05 - 0 , 0125 0 , 05 = 75 %
● Cách 2: Sử dụng phương pháp bảo toàn nguyên tố
Sơ đồ phản ứng :
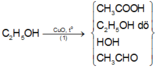
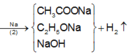
Bản chất phản ứng (1) là C 2 H 5 OH bị oxi hóa bởi CuO, khối lượng hỗn hợp sau phản ứng tăng lên là do O trong CuO chuyển vào H 2 O và CH 3 COOH . Ở phản ứng (2), CH 3 COOH , C 2 H 5 OH dư, HOH có nguyên tử H linh động trong nhóm –OH nên tham gia phản ứng thế Na giải phóng H 2 , CH 3 CHO không tham gia phản ứng này.
Sử dụng bảo toàn nguyên tố O trong phản ứng oxi hóa ancol và bảo toàn nguyên tố H của nhóm –OH trong phản ứng của X với Na, ta có :
n HOH = n CH 3 COOH = n O pư = 0 , 0625 n HOH + n CH 3 COOH + n C 2 H 5 OH dư = 2 n H 2 = 0 , 075 ⇒ n C 2 H 5 OH dư = 0 , 0125 H = 0 , 05 - 0 , 0125 0 , 05 = 75 %

Chọn đáp án D.
Muối của axit hữu cơ thu được là duy nhất Þ ancol và anđehit có cùng số nguyên tử C.
Þ Đặt CTTQ của ancol là; RCH2OH (x mol), của anđehit là RCHO (y mol)
Áp dụng định luật bảo toàn nguyên tố ta có:
x + y = n N a O H + 2 n N a 2 C O 3 = 4 % .100 40 + 2. 26 , 5 % .100 106 = 0 , 6 mol 1 ⇒ M ¯ X = 26 , 6 0 , 6 = 44 , 33 ⇒ R + 29 < 44 , 33 < R + 31 ⇒ 13 , 33 < R < 15 , 33 ⇒ R = 15 C H 3 − ⇒ m x = 46 x + 44 y = 26 , 6 g 2
Từ (1) và (2) ⇒ x = 0 , 1 m o l v à y = 0 , 5 m o l
⇒ % m C 2 H 5 O H = 46.0 , 1.100 % 26 , 6 = 17 , 29 %

![]()
Vì thu được dung dịch chỉ chứa một muối của axit hữu cơ nên
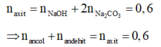
Gọi công thức của ancol và anđehit lần lượt là RCH2OH và RCHO.
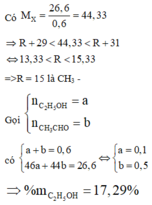
Đáp án D

Chọn đáp án D.
Quy đổi hỗn hợp T tương đương với hỗn hợp gồm CnH2n+2O (x mol); CmH2m-6O6 (y mol).
n
C
O
2
=
a
n
H
2
O
=
a
+
0
,
03
→
B
T
K
L
26
,
86
+
32.1
,
425
=
44
a
+
18.
a
+
0
,
03
⇒
a
=
1
,
16
→
B
T
N
T
O
x
+
6
y
=
2.1
,
16
+
0
,
03
+
1
,
16
−
2.1
,
425
=
0
,
66
m
o
l
1
14
n
+
18
x
+
14
m
+
90
y
=
26
,
86
g
⇒
14.
n
x
+
m
y
+
18
x
+
90
y
=
14.1
,
16
+
18
x
+
90
y
=
26
,
86
2
Từ (1) và (2) suy ra:
x
=
0
,
24
y
=
0
,
07
Ancol + K dư:
∑
n
a
n
c
o
l
=
3
n
e
s
t
e
+
n
a
n
c
o
l
=
2
n
H
2
=
2.0
,
18
=
0
,
36
m
o
l
n
e
s
t
e
=
0
,
36
−
0
,
24
3
=
0
,
04
m
o
l
⇒
n
a
x
i
t
=
0
,
07
−
0
,
04
=
0
,
03
m
o
l
Ancol + AgNO3/NH3 dư:
n
A
g
=
129
,
6
108
=
1
,
2
m
o
l
⇒
2
<
n
A
g
∑
n
a
n
c
o
l
=
1
,
2
0
,
36
<
4
Þ Chứng tỏ A là CH3OH, kí hiệu ancol B, C là RCH2OH
⇒ ∑ n a n c o l = n C H 3 O H + n R C H 2 O H = 0 , 36 m o l n A g = 4 n C H 3 O H + 2 n R C H 2 O H = 1 , 2 m o l ⇒ n C H 3 O H = 0 , 24 m o l n R C H 2 O H = 0 , 12 m o l
Vậy T gồm: C H 3 O H : 0 , 24 − 0 , 04 = 0 , 2 m o l R C H 2 O H : 0 , 12 − 0 , 04.2 = 0 , 04 m o l a x i t : 0 , 03 m o l e s t e : 0 , 04 m o l
Bảo toàn nguyên tố C: 0 , 2.1 + 0 , 04. C B , C + 0 , 04. C D + 1 + 2 C B , C + 0 , 03. C D = 1 , 16
⇒ 0 , 12 C B , C + 0 , 07 C D = 0 , 92
C B , C > 2 ⇒ C D < 0 , 92 − 0 , 12.2 0 , 07 = 9 , 7 m à C D ≥ 8
⇒ C D = 8 C D = 9 ⇒ D : C 8 H 10 O 6 D : C 9 H 12 O 6 ⇒ % m D = 202.0 , 03 26 , 86 .100 % = 22 , 56 % % m D = 216.0 , 03 26 , 86 .100 % = 24 , 13 %



Chọn đáp án A.