Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích:
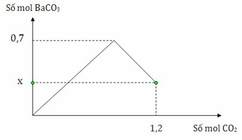
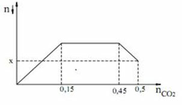
Quan sát đồ thị ta thấy nCO2 = 0,15 thì kết tủa đạt max.
=> nCa(OH)2 = nCaCO3 max = 0,15
Khi nCO2 = 0,45 thì bắt đầu hòa tan kết tủa.
Khi nCO2 = 0,5 thì lượng kết tủa bị hòa tan là: nCaCO3 bị hòa tan = 0,5 - 0,45 = 0,05
=> nCaCO3 còn lại = x = 0,15 - 0,05 = 0,1
Đáp án A

Đáp án B.
Cách 1:
Tại A:
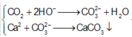
![]()
Quá trình
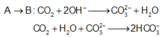
Tại C:
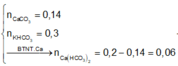
![]()
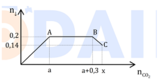
Cách 2: Phân tích đồ thị:
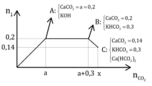
x = 0,2 + 0,3 + (0,2 - 0,14) = 0,56

Đáp án C
Cách 1:
Tại A: CO2 + 2OH− → CO2−3 + H2O
Ba2+ + CO2−3 → BaCO3↓
n B a C O 3 = a m o l
Quá trình A → B: CO2 + 2OH− → CO2−3 + H2O
CO2 + H2O + CO2−3 → 2HCO−3
Khối lượng kết tủa không đổi
![]()
Tại C:
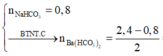
![]()
a + b = 0,8 + 0,8 = 1,6
Cách 2: Phân tích đồ thị
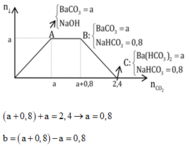

Đáp án D
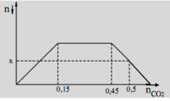
Nhận thấy đồ thị có các giai đoạn:
+Giai đoạn kết tủa tăng dần do Ca(OH)2 tác dụng với CO2 tạo kết tủa CaCO3.
+Giai đoạn kết tủa không đổi do CO2 tác dụng với KOH.
+Giai đoạn kết tủa giảm dần do CO2 tác dụng với CaCO3 và hòa tan kết tủa này (tạo Ca(HCO3)2).
![]()
Lúc CO2 đạt 0,5 mol thì kết tủa đã bị hòa tan mất 0,05 mol (do từ 0,45 mol đã bắt đầu hòa tan kết tủa).
=> x = 0,15 - 0,05 = 0,1 mol

Chọn đáp án A
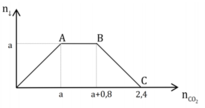
nCa(OH)2 = nCaCO3 max = a mol ⇒ nOH– = 2a mol.
Khi kết tủa bị hòa tan 1 phần thì: nCO32– = nOH– - nCO2.
► Áp dụng: + Tại 0,06 mol CO2: 2b = 2a - 0,06.
+ Tại 0,08 mol CO2: b = 2a - 0,08. Giải hệ có:
a = 0,05 mol; b = 0,02 mol ⇒ a : b = 5 : 2 ⇒ chọn A.

Chọn đáp án C
nOH– = 4nAl3+ – n↓ ⇒ x = nAl3+ = (0,1 + 0,5) ÷ 4 = 0,15 mol ⇒ chọn C.

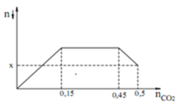
Giải thích:
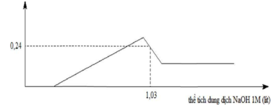
Cho từ từ đến dư NaOH vào AlCl3 ta có:
Kết tủa cực đại khi tất cả Al3+ chuyển thành Al(OH)3
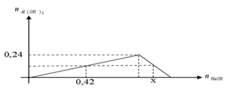
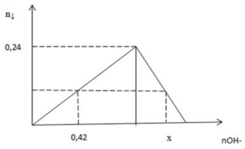
Từ đồ thị: nAl(OH)3 max = 0,24 (mol) => nAl3+ ban đầu = 0,24 (mol)
+ nOH- = 0,42 mol => chỉ tạo kết tủa Al(OH)3. Khi đó nAl(OH)3 = 1/3nOH- = 1/3. 0,42 = 0,14 (mol) (1)
+ nOH- = x mol => tạo kết tủa Al(OH)3 cực đại sau đó kết tủa Al(OH)3 tan dần đến khi còn lại đúng 1 lượng như ở (1)
Al3+ + 3OH- → Al(OH)3↓
0,14← 0,42 ← 0,14
Al3+ + 4OH- → AlO2- + H2O
(0,24- 0,14)→ 0,4
∑ nOH- = 0,42 + 0,4 = 0,82 (mol)
Đáp án A
Đáp án cần chọn là: A