Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(n_K=\dfrac{0,975}{39}=0,025\left(mol\right)\)
A là khí H2, B là CH3COOK
PTHH: 2K + 2CH3COOH → 2CH3COOK + H2
Mol: 0,025 0,025 0,0125
b, \(C_{M_{ddCH_3COOH}}=\dfrac{0,025}{0,1}=0,25M\)
c, \(V_{H_2}=0,0125.22,4=0,28\left(l\right)\)

Đáp án A
Ta có : nCuO ban đầu= 0,04 mol ; nHCl= 0,02 mol
2NH3+ 3CuO → t o N2+ 3Cu + 3H2O (1)
CuO + 2HCl→ CuCl2+ H2O (2)
Theo PT (2) nCuO PT2= ½.nHCl= 0,01 mol
→nCuO PT 1= nCuO- nCuO PT2= 0,04-0,01=0,03 mol
→ nN2=1/3.nCuO PT1= 0,01 mol
→ VN2=0,224 lít

Đáp án D
• 0,42 mol NaOH + 0,02 mol Fe2(SO4)3; 0,04 mol Al2(SO4)3 → 500ml X + ↓
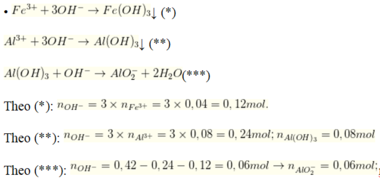
nAl(OH)3 = 0,08 - 0,06 = 0,02 mol
Vậy sau phản ứng 500ml dung dịch X gồm 0,06 mol Na[Al(OH)4]; 0,18 mol Na2SO4
→ CM các chất trong X là CMNa2SO4 = 0,06 : 0,5 = 0,12 M;
CMNa[Al(OH)4] = 0,18 : 0,5 = 0,36 M

1. Phương trình hoá học của các phản ứng :
2 N H 3 + 3CuO → t ° N 2 + 3Cu + 3 H 2 O (1)
Chất rắn A thu được sau phản ứng gồm Cu và CuO còn dư. Chỉ có CuO phản ứng với dung dịch HCl :
CuO + 2HCl → C u C l 2 + H 2 O (2)
2. Số mol HCl phản ứng với CuO : n H C l = 0,02.1 = 0,02 (mol).
Theo (2), số mol CuO dư : n C u O = n H C l / 2 = 0,01 (mol).
Số mol CuO tham gia phản ứng (1) = số mol CuO ban đầu - số mol CuO dư = 0,03 (mol).
Theo (1) n N H 3 = 2 n C u O /3 = 0,02 (mol) và nN2 = n C u O /3 = 0,01 (mol).
Thể tích khí nitơ tạo thành : 0,01. 22,4 = 0,224 (lít) hay 224 ml.
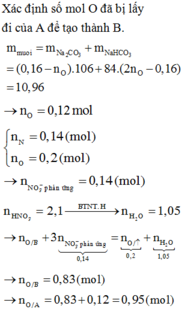

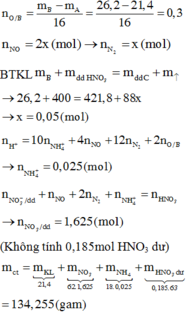

bạn ơi bạn thiếu nồng độ mol của etanol thì làm sao tính được số mol của nó ạ?