
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt

Tham khảo:
- Hiện tượng: Nước bromine mất màu và xuất hiện kết tủa trắng.
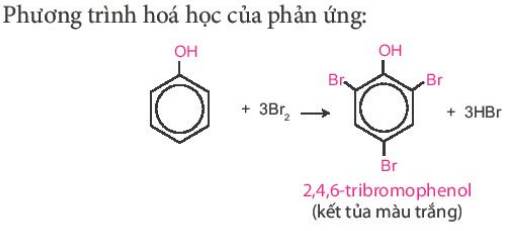
- Giải thích: Phenol phản ứng bromine, làm nước bromine mất màu, tạo kết tủa trắng 2,4,6-tribromophenol.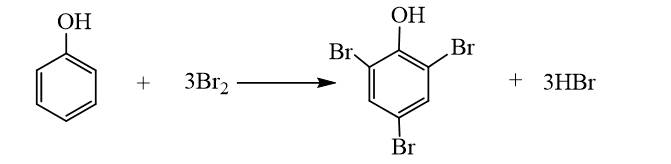
Hiện tượng:
-Nước brom mất màu
-Xuất hiện kết tủa trắng
Giải thích: Khi phenol phản ứng với brom thì sẽ làm mất màu nước brom và sẽ tạo ra kết tủa trắng 2,4,6-tribromophenol

Tham khảo:
- Phenol ít tan trong nước lạnh.
- Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt.
- Giải thích: Phenol phản ứng với dung dịch sodium hydroxide tạo thành dung dịch muối tan trong suốt sodium phenolate (C6H5ONa).
C6H5OH + NaOH → C6H5ONa + H2O
Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt
Giải thích: Phenol khi tác dụng với NaOH sẽ cho ra dung dịch muối tan trong suốt là C6H5ONa

Hiện tượng: Cả 2 ống nghiệm đều xuất hiện kết tủa xanh lam nhạt (Cu(OH)2)
PTHH: CuSO4 + 2 NaOH → Cu(OH)2↓(xanh) + Na2SO4 (PTHH ở bước 2)
- Khi cho gylycerol vào ống 1: Kết tủa tan tạo thành dung dịch màu xanh lam của muối copper(II) glycerate
PTHH: 2 C3H5(OH)3 + Cu(OH)2→ [C3H5(OH)2O]2Cu + 2 H2O
- Khi cho ethanol vào ống 2: không có hiện tượng, kết tủa không tan.
Hiện tượng
-Khi cho vào hai ống nghiệm dung dịch CuSO4 thì sẽ xuất hiện kết tủa màu xanh lam
-Khi cho vào ống 1 glyxerol thì sẽ làm cho kết tủa tan dần tạo dần thành dung dịch màu xanh lam
-Khi cho etanol vào ống 2 thì kết tủa sẽ ko tan
PTHH:
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)

Tham khảo:
- Hiện tượng: Dung dịch sau phản ứng phân thành 2 lớp, có mùi thơm nhẹ.
- Phương trình: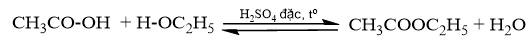
- Dấu hiệu nhận biết có sản phẩm mới được tạo thành: Dung dịch bị phân lớp, xuất hiện mùi. Vì ester sinh ra ít tan trong nước, nhẹ hơn nước, nổi lên trên và có mùi thơm đặc trưng.

Đáp án: B
TN1:
CH2 = CH – CH2Cl + H2O → CH2 = CH – CH2OH + HCl
TN2:
CH2 = CH – CH2Cl + NaOH → CH2 = CH – CH2OH + NaCl
Cả hai dung dịch đều chứa ion Cl– nên đều tạo kết tủa trắng với AgNO3

Hiện tượng: Thấy có lớp chất lỏng nặng màu vàng nhạt, sánh như dầu lắng xuống.

Tham khảo:
- Khi nhỏ vài giọt dung dịch acetic acid lên mẩu giấy quỳ tím, mẩu quỳ tím hóa đỏ vì acetic acid có tính acid.
- Khi cho vào ống nghiệm thứ nhất chứa dung dịch acetic acid vài mẩu magnesium, mẩu magnesium tan và xuất hiện bọt khí.
→ Giải thích: Acetic acid phản ứng với magnesium, làm magnesium tan và tạo khí hydrogen.
2CH3COOH + Mg → 2(CH3COO)2Mg + H2↑
- Khi cho vào ống nghiệm thứ hai chứa acetic acid 1 thìa sodium carbonate, sodium carbonate tan và xuất hiện bọt khí.
→ Giải thích: Acetic acid phản ứng với sodium carbonate, sinh ra khí carbon dioxide.
2CH3COOH + Na2CO3 → 2CH3COONa + H2O + CO2↑

Bài 6:
KMnO4 và HCl trong thí nghiệm được dùng để điều chế chlorine
2 KMnO4 + 16 HCl → 2 KCl + 2 MnCl2 + 5 Cl2 + 8 H2O
Bài 5:
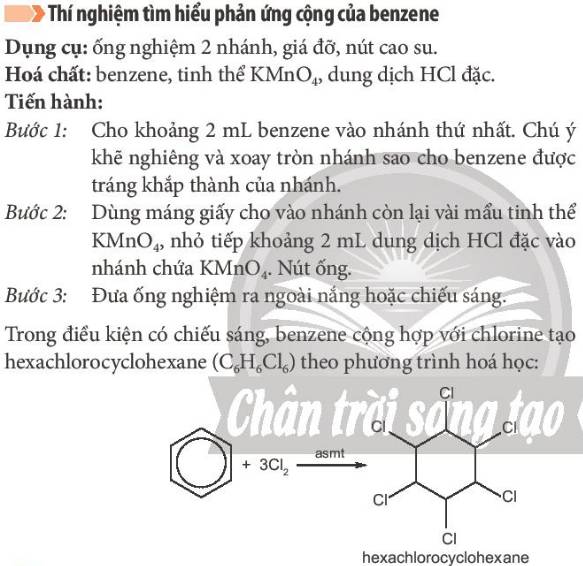
Hiện tượng: xuất hiện khói trắng, trên thành thấy xuất hiện một lớp bột màu trắng (Hexachlorocyclohexane).
C6H6 + 3 Cl2 -> (as) C6H6Cl6











Cồn cháy được tạo thành khí không màu và hơi nước.
Hiện tượng là etanol cháy tạo thành ngọn lửa màu vàng và nó sẽ tỏa nhiệt rất nhiều