Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Lượng NaOH dùng khác nhau nhưng lại thu được lượng kết tủa như nhau. Chứng tỏ khi cho 18 gam X vào 400 ml AlCl 3 0,1M (TN1) thì Al 3 + chưa phản ứng hết, còn khi cho 74 gam X vào 400 ml AlCl 3 0,1M (TN2) thì Al 3 + bị kết tủa hết, sau đó một phần Al OH 3 bị hòa tan. Ta có :
n NaOH TN 1 n NaOH TN 2 = m dd NaOH TN 1 m dd NaOH TN 2 = 18 74 ⇒ n dd NaOH TN 1 = 18 x n dd NaOH TN 2 = 74 x
Đặt ![]()
Theo bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
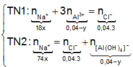
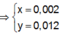
![]()

Đáp án D
► Bảo toàn electron: 3nAl = 2nH2 ⇒ nAl = 0,02 mol.
"vừa đủ" ⇒ X chỉ chứa AlCl3 || 0,09 mol hay 0,13 mol NaOH cho cùng 1 lượng ↓
⇒ 0,09 mol NaOH thì ↓ chưa đạt cực đại và 0,13 mol NaOH thì ↓ bị hòa tan 1 phần.
⇒ n↓ = 0,09 ÷ 3 = 0,03 mol. ||► Mặt khác, khi bị hòa tan 1 phần thì:
nOH– = 4nAl3+ – n↓ ⇒ nAl3+ = (0,03 + 0,13) ÷ 4 = 0,04 mol.
Bảo toàn nguyên tố Al: nAl2O3 = 0,01 mol ||⇒ m = 1,56(g)

Đáp án B
Gọi số mol MgSO4 và Al2(SO4)3 lần lượt là x và y (mol) có trong 200ml dung dịch.
+ 400 ml dd X + NH3 dư => kết tủa thu được là Mg(OH)2 : 2x ( mol) và Al(OH)3: 4y (mol)
=> ∑ mkết tủa = 58.2x + 78.4y = 65,36 (1)
+ 200 ml dd X + Ba(OH)2 dư => kết tủa thu được là Mg(OH)2 : x (mol) và BaSO4 : x + 3y (mol) ( Vì Al(OH)3 tan được trong dd Ba(OH)2 dư)
=> ∑ mkết tủa = 58x + (x + 3y).233 = 151,41 (2)
Từ (1) và (2) => x = 0,16 ; y = 0,15
+ 500 ml dd X ( có 0,4 mol Mg2+, 0,75 mol Al3+) + NaOH→ 70gam kết tủa => lượng NaOH lớn nhất ứng với trường hợp tạo Mg(OH)2↓ và Al(OH)3↓ sau đó kết tủa bị hòa tan 1 phần
=> nAl(OH)3 = (70 – 0,4.58)/78 = 0,6 (mol)
Mg2+ + 2OH → 2Mg(OH)2↓
0,4 → 0,8 (mol)
Al3+ + 3OH-→ Al(OH)3↓
0,75→2,25 → 0,75 (mol)
Al(OH)3+ OH- → AlO2- + 2H2O
(0,75-0,6) → 0,15 (mol)
∑ nOH-= 0,8 + 2,25 + 0,15 = 3,2 (mol) =nNaOH
=> mNaOH = 3,2.40 = 128 (g)

X có CTPT C 3 H 12 N 2 O 3 . X tác dụng với dung dịch NaOH (đun nóng nhẹ) hoặc HCl đều có khí thoát ra
=> X chỉ có thể là muối của H 2 C O 3 và amin
→ X là N H 4 O − C O O N H 3 C 2 H 5
( N H 4 ) ( N H 3 C 2 H 5 ) C O 3 + 2 N a O H → N a 2 C O 3 + N H 3 + C 2 H 5 N H 2 + 2 H 2 O
n X = 0 , 15 m o l ; n N a O H = 0 , 4 m o l
=> NaOH dư 0,1 mol
=> m = m N a O H d d + m N a 2 C O 3 = 19 , 9 g a m
Đáp án cần chọn là: C
Chú ý
+ Quên không tính khối lượng NaOH dư → chọn nhầm A

nOH- = 0,04 mol
Vì nAlO2- = 0,02 mol mà chỉ thu được 0,01 mol kết tủa nên nHCl = 4n kết tủa + nAlO2- dư = 0,05 mol
=> tổng nH+ = 0,09 mol => V = 45ml
Vậy : B đúng
H+ + OH- => H2O 1
0,02......0,02
H+ + AlO2 - + H2O => Al(OH)3 2
0,02.....0,02.........................0,02
3H+ + Al(OH)3 => Al3+ +3H2O 3
0,03.........0,01
do cần V lớn nhất nên xét TH tạo kết tủa xong hòa tan 1 phần kết tủa
n Al(OH)3 =0,01 => nAl(OH)3 ở 3 =0,01
=> nHCl= 0,03 +0,02 +0,02 =0,07 => V=0,035 => C

Đáp án A
Định hướng tư duy giải
Dùng kỹ thuật trừ phân tử suy ra X là (CH3NH3)2CO3
Ta có:
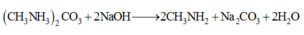
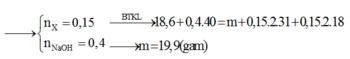

Đáp án A

![]()
Suy ra được 2 muối ![]()
Gọi số mol của mỗi muối là a;b

![]()
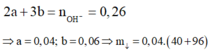
![]()

Ta có nH2 = 0,4 mol; nAl2(SO4)3 = 0,04 mol
Gọi x = nBa ⇒ nK = 2x
Ba + 2H2O → Ba(OH)2 + H2
x → x → x
K + H2O → KOH + H2
2x → 2x → x
Ta có nH2 = x + x = 0,4 x = 0,2
⇒ nOH- = 2nBa(OH)2 + nKOH = 2x + 2x = 0,8 mol
nAl3+ = 2nAl2(SO4)3 = 0,08; nSO42- = 3nAl2(SO4)3 = 0,12 mol; nBa2+ = nBa(OH)2 = 0,2 mol
Ba2+ + SO42- → BaSO4↓
(0,2) (0,12) → 0,12 mol
Al3+ + 3OH- → Al(OH)3↓
0,08 → 0,24 → 0,08
Như vậy nOH- còn dư = 0,8 – 0,24 = 0,56 mol
Al(OH)3 + OH- còn dư → AlO2- + 2H2O
0,08 → 0,08
Sau khi kết thúc phản ứng, OH- vẫn còn dư và kết tủa thu được chỉ có BaSO4
⇒ m = mBaSO4 = 233.0,12 = 27,96g ⇒ Chọn D.

Đáp án B
Theo giả thiết, ta có :
Dựa vào bản chất phản ứng và giả thiết, ta có đồ thị :
Dựa vào tính chất hình học của đồ thị, ta có :
0,16 - 37x = 3x => x = 0,004 ⇒ C % = 0 , 004 . 9 . 40 18 = 8 % ⇔ C = 8