

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



B
Nếu A và B cùng là nguyên tố s hoặc p.
Nếu A ít hơn B 1 lớp electron thì A có thể ít hơn B là 2 hoặc 8 hoặc 18 electron
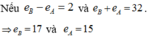
(loại vì 2 nguyên tố này có cùng lớp electron).
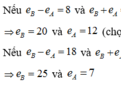
(loại vì 2 nguyên tố này khác nhau 2 lớp electron).
Vậy A và B có 2 electron ở lớp ngoài cùng.

1.Nguyên tử của nguyên tố X có phân lớp electron ngoài cùng là 3p4. Phát biểu nào sau đây không đ ng?
A. X có 4 electron ở lớp ngoài cùng.
B. X là phi kim.
C. X có 3 lớp electron.
D. Số hạt mang điện của nguyên tử X là 32
\(1s^22s^22p^63s^23p^4\) => Z= 16, có 6e lớp ngoài cùng
2. Nguyên tử R có cấu hình eletron: 1s22s22p63s23p5. Nhận xét nào dưới đây sai khi nói về R?
A. Số hiệu nguyên tử của R là 17 B. R có 3 lớp e
C. R có 5e ở lớp ngoài cùng. (3s23p5=>7e ngoài cùng) D. R là phi kim
3.Phát biểu nào dưới đây là ĐÚNG?
A. Electron ở phân lớp 4p có mức năng lượng thấp hơn electron ở phân lớp 4s.
B. Những electron ở gần hạt nhân có mức năng lượng cao nhất.
C. Những electron ở lớp K có mức năng lượng thấp nhất.
(Theo trình tự sắp xếp lớp K là lớp gần hạt nhân nhất. Năng lượng của electron trên lớp K là thấp nhất.)
D. Các electron trong cùng một lớp có năng lượng bằng nhau.
4. Nhận định nào ĐÚNG?
A. Nguyên tố có số hiệu nguyên tử bằng 5 là nguyên tố kim loại.
B. Nguyên tố mà nguyên tử có 7 electron ở lớp ngoài cùng thường là phi kim.
C. Các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng.
D. Tất cả các nguyên tố s đều là nguyên tố kim loại.
5. Số phân lớp, số obitan và số electron tối đa của lớp M lần lượt là
A. 3 ; 3 ; 6.
B. 3 ; 6 ; 12.
C. 3 ; 9 ; 18.
D. 4 ; 16 ; 18.
- Lớp M :3 phân lớp: 3s, 3p, 3d
- Phân lớp M chứa tối đa 18 electron
- Số obitan trong lớp e thứ n là n2 obitan =32 =9