Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B
Chuyển dịch sang một trạng thái cân bằng mới, nhiệt độ không đổi → Kc không đổi.
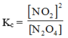
→ nồng độ của N 2 O 4 tăng lên 9 lần thì nồng độ của N O 2 tăng 3 lần

Đáp án B.
Vt = k[N2O4], Vn = k[NO2]2
ở trạng thái cân bằng. Vt = Vn
Nên khi tăng nồng độ của N2O4 lên 9 lần thì nồng độ của NO2 tăng 3 lần

Đáp án D
Hằng số cân bằng: 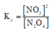
Khi tăng nồng độ N2O4 lên 9 lần đê’hằng số K không đổi thì nồng độ NO2 phải tăng lên 3 lần

Đáp án D
Hằng số cân bằng: K c = [ NO 2 ] 2 [ N 2 O 4 ]
Khi tăng nồng độ N2O4 lên 9 lần đê’hằng số K không đổi thì nồng độ NO2 phải tăng lên 3 lần.

Khi tăng nhiệt độ, cân bằng hoá học của phản ứng sẽ chuyển sang chiều nghịch. Bởi vì phản ứng thuận toả nhiệt

Chọn đáp án A
1) Không dịch chuyển
2) Dịch qua phải
3) Dịch qua trái
4) Không dịch chuyển
5) Dịch qua phải

Chọn đáp án B
Muốn cân bằng không dịch chuyển khi tăng áp thì tổng số mol khí không đổi sau phản ứng:
1) Fe2O3(r) + 3CO(k) ⇌ 2Fe(r) + 3CO2(k) (Thỏa mãn 3 =3 )
2) CaO(r) + CO2(k) ⇄ CaCO3(r) (Không thỏa mãn 1 ≠0)
3) N2O4(k) ⇄ 2NO2(k) (Không thỏa mãn 1 ≠2)
4)H2(k) + I2(k) ⇄ 2HI(k) (Thỏa mãn 2 =2 )
5) 2SO2(k) + O2(k) ⇄ 2SO3(k) (Không thỏa mãn 3 ≠2)

Khi tăng áp suất chung, cân bằng hoá học của phản ứng sẽ chuyển sang chiều thuận. Bởi vì sau phản ứng thuận có sự giảm thể tích khí.

Nhận thấy trong phản ứng (1) tổng số mol khí trước = tổng số mol khí nên áp suất không ảnh hưởng đến cân bằng.
Khi tăng áp suất thì cân bằng chuyển dịch theo hướng làm giảm số mol khí
(2) chuyển dịch theo chiều thuận
(3), (4), (5), (6) chuyển dịch theo chiều nghịch
Đáp án B
Chọn đáp án B
Gọi nồng độ của N2O4 và NO2 ban đầu lần lượt là a, x.
Sau khi tăng nồng độ của N2O4 là 9a, của NO2 là y: nên