hỗn hợp A gồm 3 khí H2, H2S, SO2 có tỷ lệ mol tương ứng là 1:2:3. Trộn A với O2 dư trong bình kín xúc tác V2O5 rồi đốt cháy hoàn toàn A, làm lạnh hỗn hợp sau phản ứng chỉ thu được 1 chất Y duy nhất. xác định công thức của Y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
A(H2 ; H2S ; SO2) + O2 dư => H2SO4.nSO3
Giả sử số mol các chất trong A lần lượt là t ; 2t ; 3t
=> nH = 6t ; nS = 5t
=> Theo công thức Oleum có : nH : nS = 2 : (1 + n) = 6t : 5t
=> n = 2/3
Vì các ký hiệu số đều là số nguyên nên Oleum sẽ là 3H2SO4.2SO3
=> Số nguyên tử = 29

Chọn nCO2 = 6 , nH2O = 7
Hỗn hợp Y gồm nO2 = a mol, nO3 = b mol
X + Y → CO2 + H2O
Áp dụng ĐLBT nguyên tố O: 2a + 3b = 6.2 + 7
mY = 32a + 48b = 19.2 (a+b)
=> a = 5 và b = 3
=> nX = 1/2 nY = 4 mol
=> mX = 6.44 + 7.18 - 32.5 - 48.3 = 83 gam
<=> MX = \(\dfrac{m_X}{n_X}\)= 20,75 gam/mol
<=> d\(\dfrac{X}{H_2}\)= 20,75:2 = 10,375

\(\overline{M}=24\cdot2=48\)
\(\dfrac{n_{SO_2}}{n_{O_2}}=\dfrac{64-48}{48-32}=1\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(\Rightarrow n_{SO_2}=n_{O_2}=0.15\left(mol\right)\)
\(2SO_2+O_2\underrightarrow{^{t^0,V_2O_5}}2SO_3\)
Bđ:0.15....0.15
Pư: x..........0.5x......x
KT: 0.15-x..0.15-0.5x..x
\(n_{hh}=0.15-x+0.15-0.5x+x=0.3-0.5x\left(mol\right)\)
\(m=\left(0.15-x\right)\cdot64+\left(0.15-0.5x\right)\cdot32+80x=\left(0.3-0.5x\right)\cdot2\cdot26\)
\(\Rightarrow x=\dfrac{3}{65}\)
\(H\%=\dfrac{\dfrac{3}{65}}{0.15}\cdot100\%=30.7\%\)

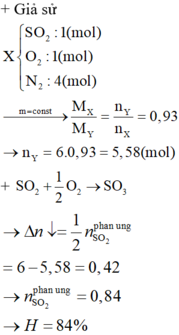
công thức Y là H2SO4 nhá!!!!
làm như nào bạn?