Trong phòng thí nghiệm, người ta điều chế Fe3O4 bằng cách dùng oxi để oxi hoá sắt ở nhiệt độ cao.
a/ Tính thể tích O2 ở ĐKTC cần dùng để điều chế được 2,32g Fe3O4.
b/ Tính số gam kalipemanganat KMnO4 cần dùng để có được lượng O2 dùng cho phản ứng trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Phương trình hóa học của phản ứng:
3Fe + 2O\(_2\) → Fe\(_3\)O\(_4\).
nFe3O4 = \(\dfrac{2,32}{232}\) = 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
a.
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,03 0,02 0,01 ( mol )
\(m_{Fe}=0,03.56=1,68g\)
\(m_{O_2}=0,02.32=0,64g\)
b.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,04 0,02 ( mol )
\(m_{KMnO_4}=0,04.158=6,32g\)

a, Ta có: \(n_{Fe_3O_4}=\dfrac{11,6}{232}=0,05\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
___0,15__0,1____0,05 (mol)
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\)
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
b, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
________0,2________________________0,1 (mol)
\(\Rightarrow m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
Bạn tham khảo nhé!

a, \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b, \(n_{Fe_2O_3}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
Theo PT: \(n_{O_2}=2n_{Fe_2O_3}=0,02\left(mol\right)\Rightarrow V_{O_2}=0,02.22,4=0,448\left(l\right)\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(2mol\) \(1mol\)
\(0,02mol\) \(0,01mol\)
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
\(V_{O_2}=n.22,4=0,02.22,4=0,048\left(l\right)\)

PTHH: \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
Ta có: \(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{O_2}=0,02\left(mol\right)\\n_{Fe}=0,03\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,03\cdot56=1,68\left(g\right)\\V_{O_2}=0,02\cdot22,4=0,448\left(l\right)\end{matrix}\right.\)

nFe3O4 = 2,32/232 = 0,01 mol
3Fe + 2O2 ➝ Fe3O4
0,03 0,02 0,01 (mol)
a) mFe = 0,03.56 = 1,68 gam
b) VO2 = 0,02.22,4 = 0,448 lít

a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 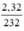 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.

PTHH: \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
Ta có; \(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,03\left(mol\right)\\n_{O_2}=0,02\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,03\cdot56=1,68\left(g\right)\\V_{O_2}=0,02\cdot22,4=0,448\left(l\right)\end{matrix}\right.\)

a,\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,03<--0,02<-------0,01
\(\left\{{}\begin{matrix}m_{Fe}=0,03.56=1,68\left(g\right)\\m_{O_2}=0,02.32=0,64\left(g\right)\end{matrix}\right.\)
b, PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,04<-----------------------------------0,02
\(m_{KMnO_4}=\dfrac{0,04.158}{85\%}=7,435\left(g\right)\)
PTHH: 3Fe + \(2O_2\) --->\(Fe_3O_4\)
theo pt: 3_____2_____________1
theo đề: x______y_____________0.01
nFe3O4 là: 0.01mol
\Rightarrow nO2= 0.01*2/1=0.02 mol
VO2= 0.02*22.4=0.448l
b, PTHH : 2KMnO4 ----> K2MnO4 + MnO2 + O2
theo pt: 2__________1________1______1
theo đề: x___________________________0.02
=> n KMnO4= 0.02*2/1= 0.04 mol
=>mKMnO4= 0.04*158=6.32g
a. số mol của Fe3O4 là :
2.32 : 232 =0.01 mol
theo tỉ lệ mol ta có số mol của Fe là:
0.01 * 3 = 0.03 mol
khối lượng sắt là: 0.03*56=1.68g
số mol oxi là: 0.01*2=0.02mol
thể tích oxi là: 0.02*22.4= 0.448g
b. 2KMnO_4 ---> K2MnO4 + MnO2 + O2
---> nKMnO_4 = 2nO2 = 0,04 mol ---> mKMnO_4=0.04*158=6.32g