Sử dụng bảng tuần hoàn, hãy xác định vị trí (số thứ tự, chu kì, nhóm) của các nguyên tố Al, Ca, Na.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Oxygen (KHHH: O):
- STT: 8
- Chu kì: 2
- Nhóm: VIA
Chlorine (KHHH: Cl)
- STT: 17
- Chu kì: 3
- Nhóm: VIIA
Sulfur (KHHH: S)
- STT: 16
- Nhóm: 3
- Chu kì: VIA
Bromine (KHHH: Br)
- STT: 35
- Chu kì: 4
- Nhóm: VIIA

- 1s22s22p4 : Nguyên tố thuộc chu kì 2 nhóm VIA.
- 1s22s22p3 : Nguyên tố thuộc chu kì 2 nhóm VA.
- 1s22s22p63s23p1 : Nguyên tố thuộc chu kì 3 nhóm IIIA.
- 1s22s22p63s23p5 : Nguyên tố thuộc chu kì 3 nhóm VIIA.

Bước 1: Viết cấu hình electron nguyên tử
- Nguyên tố X: Cấu hình electron: 1s22s22p63s23p63d14s2
- Nguyên tố Y: Cấu hình electron: 1s22s22p63s23p63d104s24p5
Bước 2: Xác định vị trí của X, Y dựa vào cấu hình electron
- Nguyên tố X: ô số 21, chu kì 4, nhóm IIIB
- Nguyên tố T: ô số 35, chu kì 4, nhóm VIIA
Chú ý: Nếu có sự chèn mức năng lượng, khi viết cấu hình electron nguyên tử cần phải đổi lại vị trí các phân lớp theo thứ tự từ trái qua phải.
Dựa vào bảng tuần hoàn (Hình 4.2), em hãy cho biết vị trí (nhóm, chu kì) của các nguyên tố K, Mg, Al
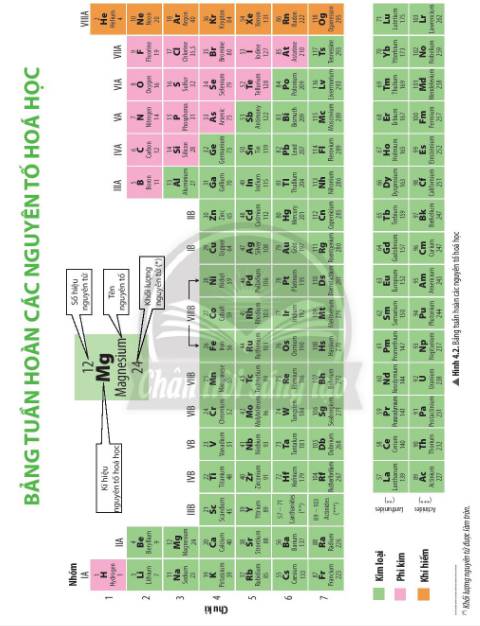

K ở nhóm IA, chu kì2
Mg ở nhóm IIA,chu kì 3
Al thuộc nhóm IIIA, chu kì 3

- Ô: Các nguyên tố hoá học được xếp theo chiều tăng dần của điện tích hạt nhân.
- Nhóm ( Cột ) : Các nguyên tố trong cùng cột có tính chất giống nhau ( đều có cùng số electron ở lớp ngoài cùng ).
- Chu kì ( Hàng ) : Các nguyên tố hoá học trong cùng hàng có cùng số lớp electron trong nguyên tử.
( Trong sách giáo khoa - Kết nối tri thức trang 24 nha )
\(#2024vv\)

Na(Z=11) 1s2 2s2 2p6 3s1 thuộc ô thứ 11, chu kì 3, nhóm IA
Al(Z=13) 1s2 2s2 2p6 3s2 3p1 thuộc ô thứ 13, chu kì 3, nhóm IIIA
S(Z=16) 1s2 2s2 2p6 3s2 3p4 thuộc ô thứ 16, chu kì 3
Nhóm VIA
Cl(Z=17) 1s2 2s2 2p6 3s2 3p5 thuộc ô thứ 17, chu kì 3,
Nhóm VIIA

a) Magnesium (Mg) thuộc ô số 12, chu kì 3, nhóm IIA trong bảng tuần hoàn.
b) Neon (Ne) thuộc ô số 10, chu kì 2, nhóm VIIIA trong bảng tuần hoàn.
a: Ô 12, chu kì 3, nhóm IIA
b: Ô 10, chu kì 2, nhóm VIIIA

Al:
- STT: 13
- Chu kì: 3
- Nhóm: IIIA
Ca
- STT: 20
- Chu kì : 4
- Nhóm: IIA
Na
- STT: 11
- Chu kì: 3
- Nhóm: IA