Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nH2 = 2,24 : 22,4 = 0,1 mol
gọi x , y lần lượt là số mol Mg và MgO
PTHH : Mg + H2SO4 → MgSO4 + H2
0,1 mol 0,1 mol 0,1 mol
=> mMg = 0,1 . 24 = 2,4 g
%mMg = \(\frac{2,4.100\%}{10,4}=23,08\text{%}\)
Ta có : mhh = mMg + mMgO
=> mMgO = 10,4 - 2,4 = 8g
=> nMgO = 8 : 40 = 0,2 mol
%mMgO = \(\frac{8.100\%}{10,4}=76,92\%\)
MgO + H2SO4 → MgSO4 + H2O
0,2 mol 0,2 mol
Số mol H2SO4 là : nH2SO4 = 0,1 + 0,2 = 0,3 mol
Nồng độ mol dd H2SO4 là
CM H2SO4 = \(\frac{0,3}{0,3}=1M\)
nH2 = 2,24 : 22,4 = 0,1 mol
PTHH : Mg + H2SO4 → MgSO4 + H2
0,1 mol 0,1 mol 0,1 mol
=> mMg = 0,1 . 24 = 2,4 g
%mMg = 2,4.100%10,4=23,08%2,4.100%10,4=23,08%
Ta có : mhh = mMg + mMgO
=> mMgO = 10,4 - 2,4 = 8g
=> nMgO = 8 : 40 = 0,2 mol
%mMgO = 8.100%10,4=76,92%8.100%10,4=76,92%
MgO + H2SO4 → MgSO4 + H2O
0,2 mol 0,2 mol
Số mol H2SO4 là : nH2SO4 = 0,1 + 0,2 = 0,3 mol
Nồng độ mol dd H2SO4 là
CM H2SO4 = 0,3.0,3=1M
#Không có gọi x,y nảy viết nhầm

Câu 1:
\(n_{H_2}=\dfrac{2.91362}{22.4}=0.13mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
2b 3b b 3b
Ta có: \(\left\{{}\begin{matrix}24a+54b=2.58\\a+3b=0.13\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.04\\b=0.03\end{matrix}\right.\)
\(m_{Mg}=0.04\times24=0.96g\)
\(m_{Al}=0.03\times2\times27=1.62g\)
\(V_{H_2SO_4}=\dfrac{0.04+3\times0.03}{0.5}=0.26l\)
Câu 2:
\(n_{H_2}=\dfrac{3.136}{22.4}=0.14mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}24a+56b=4.96\\a+b=0.14\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.09\\b=0.05\end{matrix}\right.\)
\(m_{Mg}=0.09\times24=2.16g\)
\(m_{Fe}=0.05\times56=2.8g\)
\(C\%_{H_2SO_4}=\dfrac{0.14\times98\times100}{200}=6.86\%\)
Câu 3:
\(n_{H_2}=\dfrac{1.568}{22.4}=0.07mol\)
\(Ba+H_2SO_4\rightarrow BaSO_4+H_2\)
a a a a
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}137a+24b=3.94\\a+b=0.07\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.02\\b=0.05\end{matrix}\right.\)
\(m_{Ba}=0.02\times137=2.74g\)
\(m_{Mg}=0.05\times24=1.2g\)
\(CM_{H_2SO_4}=\dfrac{0.07}{0.1}=0.7M\)

Đặt \((n_{MgO};n_{CuO})=(a;b)\)
\(MgO+H_2SO_4\to MgSO_4+H_2O\\ CuO+H_2SO_4\to CuSO_4+H_2O\\ \Rightarrow n_{MgSO_4}:n_{CuSO_4}=1:1=a:b\\ \Rightarrow a=b\)
Mà \(a+b=n_{H_2SO_4}=1.0,3=0,3(mol)\)
\(\Rightarrow a=b=0,15(mol)\\ \Rightarrow m_{MgO}=0,15.40=6(g)\)

Gọi số mol CH 3 COOH là x
số mol CH 3 COO C 2 H 5 là y.
Phương trình hoá học của phản ứng giữa axit và este với NaOH :
CH 3 COOH + NaOH → CH 3 COONa + H 2 O
x mol x mol
CH 3 COO C 2 H 5 + NaOH → CH 3 COONa + C 2 H 5 OH
y mol y mol y mol
Số mol NaOH phản ứng là : x + y = 300/1000 x 1 = 0,3 mol
Phương trình hoá học của phản ứng giữa rượu etylic với Na :
2 C 2 H 5 OH + Na → 2 C 2 H 5 ONa + H 2
y y/2
Ta có y/2 = 2,24/22,4 = 0,1 => y = 0,2
Thay y = 0,2 vào phương trình x + y = 0,3, ta có :
x = 0,3 - 0,2 = 0,1 (mol).
Vậy khối lượng axit axetic là : 60 x 0,1 = 6 (gam). Khối lượng etyl axetat là : 88 x 0,2 = 17,6 (gam).
Khối lượng hỗn hợp là : 6 + 17,6 = 23,6 (gam).
Vây % khối lương axit axetic = 6/23,6 × 100% = 25,42%
% khối lượng etyl axetat là 100% - 25,42% = 74,58%.

\(a.n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ Đặt:\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ \rightarrow\left\{{}\begin{matrix}27a+24b=5,1\\1,5a+b=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \left\{{}\begin{matrix}\%m_{Al}=\dfrac{27.0,1}{5,1}.100\approx52,941\%\\\%m_{Mg}\approx47,059\%\end{matrix}\right.\)
\(b.m_{ddH_2SO_4}=\dfrac{0,25.98.100}{9,8}=250\left(g\right)\\ m_{ddsau}=m_{Al,Mg}+m_{ddH_2SO_4}-m_{H_2}=5,1+250-0,25.2=254,6\left(g\right)\\ C\%_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,05.342}{254,6}.100\approx6,716\%\\ C\%_{ddMgSO_4}=\dfrac{0,1.120}{254,6}.100\approx4,713\%\)

Câu 5 :
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1 0,1
\(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,15 0,3 0,15
a) \(n_{Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Mg}=0,1.24=2,4\left(g\right)\)
\(m_{MgO}=8,4-2,4=6\left(g\right)\)
0/0Mg = \(\dfrac{2,4.100}{8,4}=28,57\)0/0
0/0MgO = \(\dfrac{6.100}{8,4}=71,43\)0/0
b) Có : \(m_{MgO}=6\left(g\right)\)
\(n_{MgO}=\dfrac{6}{40}=0,15\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,2+0,3=0,5\left(mol\right)\)
\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
\(m_{ddHCl}=\dfrac{18,25.100}{3,65}=500\left(g\right)\)
\(n_{MgCl2\left(tổng\right)}=0,1+0,15=0,25\left(mol\right)\)
⇒ \(m_{MgCl2}=0,15.95=14,25\left(g\right)\)
\(m_{ddspu}=8,4+500-\left(0,1.2\right)=508,2\left(g\right)\)
\(C_{MgCl2}=\dfrac{14,25.100}{508,2}=2,8\)0/0
Chúc bạn học tốt

nH2=2.24/22.4=0.1 mol
pt: Mg+2HCL->MgCl2+H2
nMg=nH2=0.1 mol
mMg=0.1*24=2.4g
=>mMg=6-2.4=3.6g
%mMg=(3.6/6)*100=60%

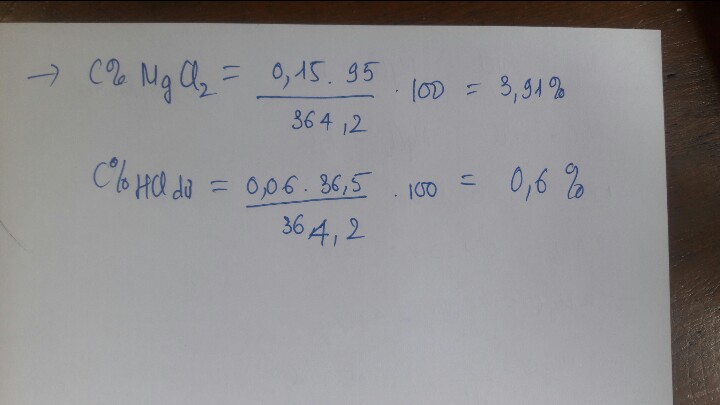
nH2SO4 = 0,3 . 1 = 0,3 mol
gọi x , y lần lượt là số mol của Mg và MgO
PTHH : Mg + H2SO4 → MgSO4 + H2
x mol x mol x mol
MgO + H2SO4 → MgSO4 + H2O
y mol y mol
Ta có hpt: \(\begin{cases}24x+40y=10,4\\x+y=0,3\end{cases}\)
Giải hpt ta đc : x= 0,1 và y = 0,2
Thể tích khí H2 thoát ra là VH2 = 0,1 . 22,4 = 2,24 lit
%mMg = \(\frac{24.0,1.100\%}{10,4}\) = 23,08%
%mMgO = \(\frac{40.0,2.100\%}{10,4}\) = 76,92%
Có cách nào làm mà k phải giải hệ phương trình kh pn