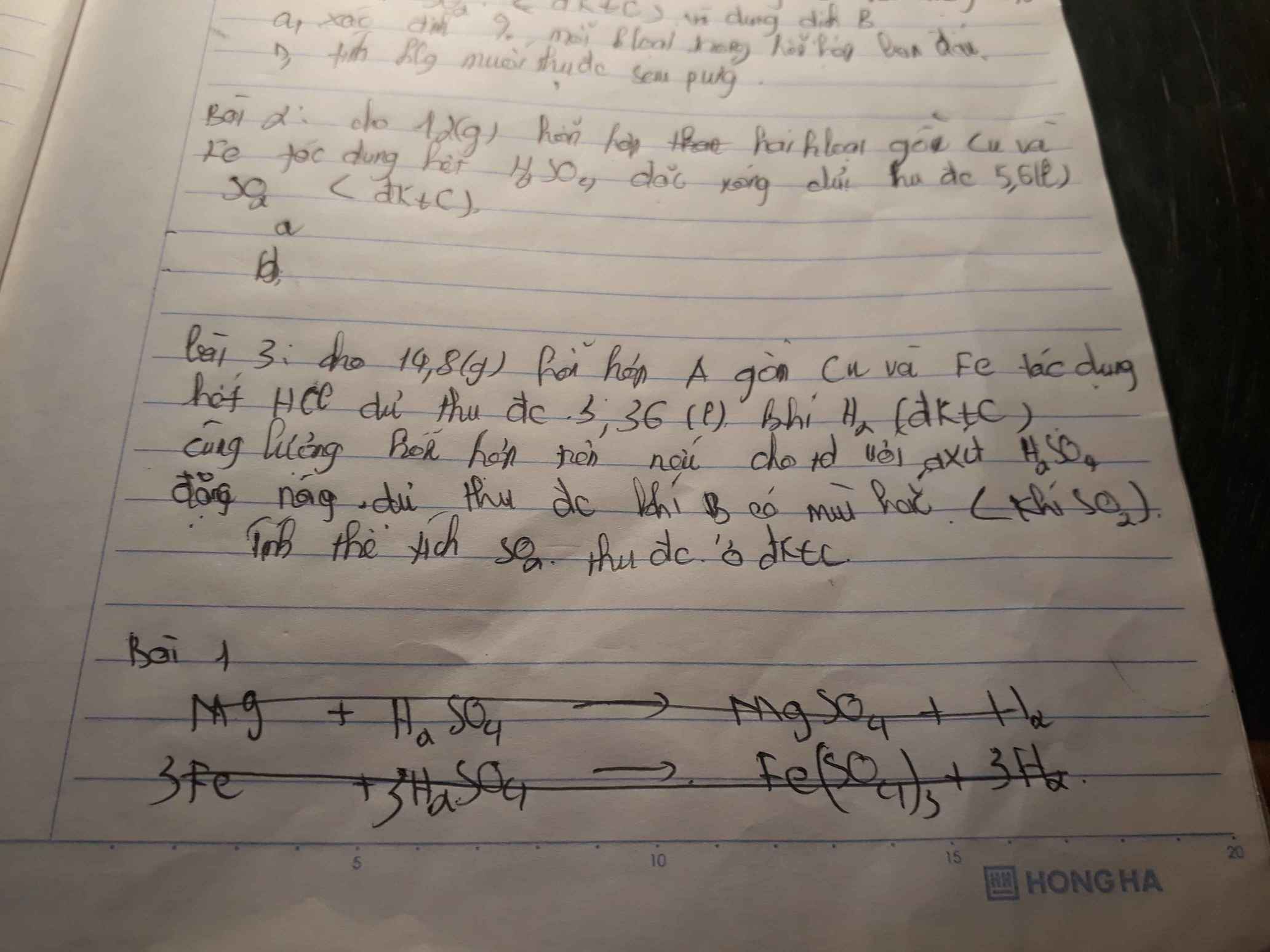Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




Bài 3 :
\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ \Rightarrow n_{Fe} = \dfrac{14,8-0,15.56}{64} = 0,1(mol)\\ Fe^0 \to Fe^{+3} + 3e\\ Cu^{0} \to Cu^{+2} + 2e\\ S^{+6} + 2e \to S^{+4}\\ n_{SO_2} = \dfrac{3n_{Fe} + 2n_{Cu}}{2} = 0,325(mol)\\ V_{SO_2} = 0,325.22,4 = 7,28(lít)\)




Chọn A.
Gọi thành phần phần trăm hai đồng vị lần lượt là a,b.
Ta có: \(\left\{{}\begin{matrix}a+b=100\%\\35a+37b=35,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=75\%\\b=25\%\end{matrix}\right.\)
Khi đó \(\%^{35}Cl=75\%\)
\(\overline{M_{FeCl_3}}=55,85+3\cdot35,5=162,35\)
\(\%^{35}Cl_{\left(trongFeCl_3\right)}=\dfrac{75\%\cdot35,5}{162,35}\approx16,4\%\)