Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Để trung hòa nửa dung dịch X cần 200ml dd HCl 0,1M
→ Để trung hòa dung dịch X cần 200 . 2 = 400ml dd HCl 0,1M
nHCl cần để trung hòa\(\text{ X = 0,4 . 0,1 = 0,04 mol}\)
nH+ = nHCl = 0,04 mol
H+ + OH- → H2O
0,04→0,04
ADĐLBT điện tích: 2 . nBa2+ + nNa+ = nNO3- + nOH-
→ nNa+ = 0\(\text{,01 + 0,04 - 0,01 . 2 = 0,03 mol}\)
Cô cạn X:
mcr = mBa2+ + mNO3- + mOH- + mNa+
\(\text{= 0,01 . 137 + 0,01 . 62 + 0,04 . 17 + 0,03 . 23}\)
\(\text{ = 3,36 (g)}\)

Đáp án A
a = nOH- = nH+ = 0,1.0,4 = 0,04 mol
BTĐT: 2nBa2+ + nNa+ = nNO3- + nOH- => 2.0,01 + b = 0,01 + 0,04 => b= 0,03
m chất rắn = 0,01.137+0,01.62+0,04.17+0,03.23=3,36 gam

\(C_{M_{HCl}}=a\left(M\right),C_{M_{H_2SO_4}}=b\left(M\right)\)
\(n_{HCl}=a\left(mol\right),n_{H_2SO_4}=b\left(mol\right)\)
\(n_{NaOH}=0.4\cdot0.5=0.2\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(a..........a.........a\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(2b............b..........b\)
\(n_{NaOH}=a+2b=0.2\left(mol\right)\left(1\right)\)
\(m_{muối}=58.5a+142b=12.95\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
\(\left[H^+\right]=0.1+0.05\cdot2=0.2\left(M\right)\)
\(\left[Cl^-\right]=0.1\left(M\right)\)
\(\left[SO_4^{2-}\right]=0.05\left(M\right)\)
\(b.\)
\(pH=-log\left(0.2\right)=0.7\)

1. Có 5 chất điện ly: NaOH, H2SO3, Na2CO3, NaCl, CH3COOH
2. A
3. Có 4 ion/ phân tử có tính axit:
HCO3- phân li thuận nghịch nấc 2, tạo H+ và CO32-
HCl phân li hoàn toàn tạo H+ và Cl-
HSO4- phân li nấc 2 tạo H+ và SO42-
NaHCO3 phân li hoàn toàn tạo Na+ và HCO3-(như trên)
Các ion khác như sau:
HPO32- không phân li được H+ nữa (H3PO3 là axit 2 nấc)
CH3COO- có tính bazo (CH3COO- + H2O ⇌ CH3COOH + OH-)
S2-, SO42- tương tự như CH3COO-, chỉ khác H2S và H2SO4 là axit 2 nấc
Cl- là ion trung tính -> Ko tác dụng với nước
Na2CO3 phân li hoàn hoàn tạo CO32- có môi trường kiềm
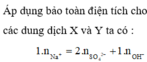

Câu 19: Cho các chất sau: Al(OH)3, HCl, KHCO3, NaCl, Na2SO4, H2SO4. Trong đó muối trung hoà gồm:A. Al(OH)3, HCl. B. NaCl, Na2SO4.C. KHCO3. D. HCl, H2SO4 Câu 20: Công thức hoá học của chất khi điện li tạo ra ion Mg2+ và Cl- làA. Mg(OH)2.B. MgCl2.C. KCl.D. MgSO4. Câu 21: Dung dịch làm quỳ tím hoá xanh làA. H3PO4.B. H2S.C. NaOH.D. HCl. Câu 22: Dung dịch H2S chứa tối đa những ion (bỏ qua sự điện li của nước):A. H+, HS-,S2-.B. HS-, S2-.C. H+, S2-.D. H+, HS-. Câu 23: Phương trình điện li nào sau đây đúng?A. CH3COOH→H+ + CH3COO-.B. HClO → H+ + ClO-.C. NaCl→ Na+ + Cl-.D. H3PO4→ H+ + H2PO42-. Câu 24: Cho 10ml dung dịch HNO3 có pH=4. Cần thêm bao nhiêu ml nước cất để thu được dung dịch có pH=6?A. 990 ml.B. 1000 ml.C. 100 ml.D. 400 ml. Câu 25: Chất nào sau đây là axit 2 nấc?A. HCl.B. Ba(OH)2.C. H2S.D. H3PO4. Câu 26: Một dung dịch chứa 0,01 mol Na+; 0,02 mol SO42-; 0,01 mol Cl- và x mol Cu2+. Giá trị của x làA. 0,04.B. 0,01.C. 0,02.D. 0,05. Câu 27: Cho các chất: NaCl, H2O, glucozơ (C6H12O6), KOH, Na2CO3, BaSO4, HF. Số chất điện li mạnh làA. 3.B. 5.C. 2.D. 4. Câu 28: Cho các cặp chất sau: (1)Na2CO3+Ba(OH)2(2) Fe + HCl (3) BaCl2 + Na2CO3(4)MgCO3+Ba(OH)2(5) CaCO3+H2SO4 Các phản ứng đều có cùng một phương trình ion rút gọn làA. (1),(2),(3),(4). B. (1),(3),(4),(5). C. (1),(3),(4). D. (1),(3).