Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Theo PTHH: \(n_{Mg}=n_{H_2}=0,6\left(mol\right)\)
=> \(m_{Mg}=0,6.24=14,4\left(g\right)\)
=> \(m_{Cu}=50-14,4=35,6\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%Mg=\dfrac{14,4}{50}.100=28,8\%\\\%Cu=\dfrac{35,6}{50}.100=71,2\%\end{matrix}\right.\)
\(n\)H2 =\(\dfrac{13,44}{22,4}\) =0,6(mol)
PTHH:
Mg +HCl →MgCl2 + H2
0,6 mol ←0,6 mol
a) \(m\)Mg =0,6. 24 =14,4(g)
\(m\)Cu= 50- 14,4= 35,6(g)
b)\(m\)%Mg= \(\dfrac{14,4}{50}\).100%= 28,8%
\(m\)%Cu=100%- 28,8%= 71,2%

ta có Cu không tác dụng với HCl nên lượng khí thoát ra là của Mg
pthh Mg + 2HCl => MgCl2 + H2
nH2 = 4.48 / 22,4 =0,2 mol mà nMg = nH2 =0,2
=> mMg= 0,2 * 24 =4,8g
mCu = 10 - 4,8 =5,2 g

a, Gọi \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
a---->1,5a--------------------------->1,5a
Mg + H2SO4 ---> MgSO4 + H2
b------>b----------------------->b
Hệ pt \(\left\{{}\begin{matrix}27a+24b=6,3\\1,5a+b=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,15\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Al}=0,1.27=2,7\left(g\right)\\m_{Mg}=0,15.24=3,6\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{2,7}{6,3}=42,86\%\\\%m_{Mg}=100\%-42,86\%=57,14\%\end{matrix}\right.\)
b, \(n_{H_2SO_4}=0,1.1,5+0,15=0,3\left(mol\right)\)
\(\rightarrow V_{ddH_2SO_4}=\dfrac{0,3}{0,5}=0,6\left(l\right)=600\left(ml\right)\)
c, đề yêu cầu jv?

nH2= \(\dfrac{0,896}{22,4}\) = 0,04(mol)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2\(\uparrow\)
a \(\rightarrow\) a (mol)
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2\(\uparrow\) (ai dạy Al hóa trị II thế =.=)
b \(\rightarrow\) 1,5b (mol)
Gọi a,b lần lượt là số mol của Mg và Al
Theo đầu bài, ta có: \(\left\{{}\begin{matrix}24a+27b=0.78\\a+1,5b=0,04\end{matrix}\right.\) \(\Rightarrow\)\(\left\{{}\begin{matrix}a=0,01\\b=0,02\end{matrix}\right.\)
=> mMg= 0,01.24 = 0,24(g)
=> mAl = 0,78 - 0,24 = 0,54(g)

a) Gọi số mol của Mg là x, của Al là y \(\left(x,y>0\right)\)
Ta có: \(24x+27y=7,8\) (*)
PTHH:
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\) (1)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\) (2)
\(n_{H_2\left(1\right)+\left(2\right)}=\dfrac{9,916}{24,79}=0,4\left(mol\right)\)
Theo PTHH: \(n_{H_2\left(1\right)}=n_{Mg}=x\left(mol\right)\); \(n_{H_2\left(2\right)}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}y\left(mol\right)\)
\(\Rightarrow x+\dfrac{2}{3}y=0,4\) (**)
Từ (*) và (**) ta có hệ:
\(\left\{{}\begin{matrix}24x+27y=7,8\\x+\dfrac{3}{2}y=0,4\end{matrix}\right.\)
Giải hệ ta được: \(\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%m_{Al}=\dfrac{27\cdot0,2\cdot100}{7,8}\approx69\%\)
\(\Rightarrow\%m_{Mg}=100\%-69\%=21\%\)
b) \(n_{MgSO_4}=n_{Mg}=0,1\left(mol\right)\); \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,1\left(mol\right)\)
Tổng khối lượng muối là:
\(m_{MgSO_4}+m_{Al_2\left(SO_4\right)_3}=0,1\cdot120+0,1\cdot342=46,2\)

a, Cu không tác dụng với dd HCl.
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,2.65=13\left(g\right)\)
\(\Rightarrow m_{Cu}=19,4-13=6,4\left(g\right)\)
c, Ta có: \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{13}{19,4}.100\%\approx67,01\%\\\%m_{Cu}\approx32,99\%\end{matrix}\right.\)
Bạn tham khảo nhé!

Lập hệ phương trình ( Al là x , Mg là y )
\(\left\{{}\begin{matrix}27x+24y=15\\27x=\dfrac{36}{100}.15\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,4\end{matrix}\right.\)
2Al + 6HCl ---> 2AlCl3 + 3H2
0,2 0,3
2Mg + 4HCl ---> 2MgCl2 + 2H2
0,4 0,4
\(\Sigma n_{H2\uparrow}=0,3+0,4=0,7\left(mol\right)\)
\(\Rightarrow V_{H2\uparrow}=0,7.22,4=15,68\left(l\right)\)
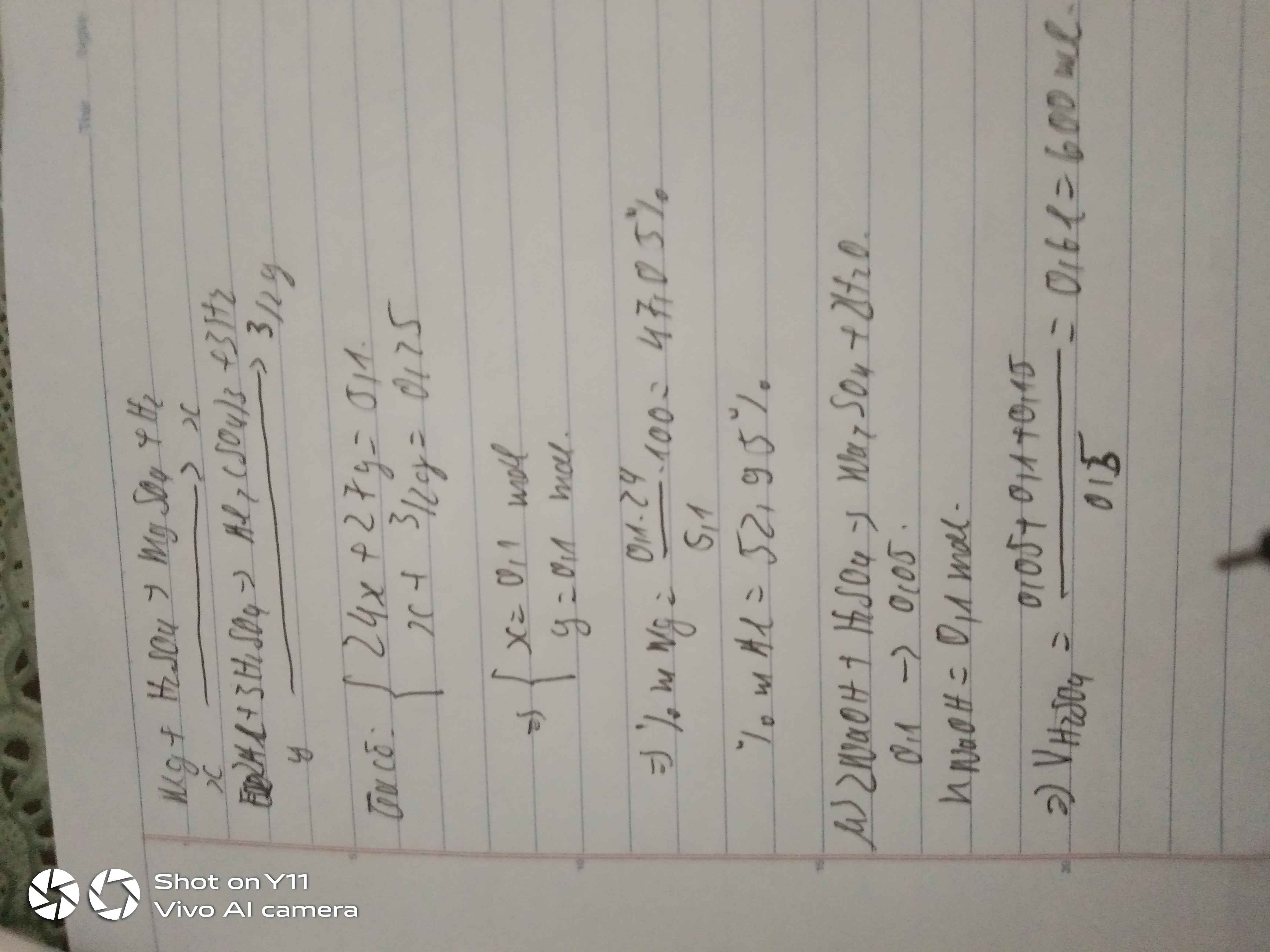
\(n_{H_2}\)= \(\dfrac{0,756}{24,79}\) = 0,0305 mol
PTHH:
Mg + 2HCl → MgCl2 + H2
Al + 3HCl → AlCl3 + \(\dfrac{3}{2}\)H2
Gọi số mol của Mg và Al lần lượt là x và y.
Ta có hệ phương trình
\(\left\{{}\begin{matrix}24x+27y=0,615\\x+1,5y=0,0305\end{matrix}\right.\)↔\(\left\{{}\begin{matrix}x=0,011\\y=0,013\end{matrix}\right.\)
⇒ mMg = 0,11 . 24 = 0,264 gam
⇒ %Mg = \(\dfrac{0,264}{0,615}\) . 100 = 43%
Phần trăm khối lượng của Mg trong hỗn hợp là 58,54%.