Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Khi cho từ từ HCl và X, đã có phương trình tạo khí
H+ + HCO3- → CO2 + H2O
Dung dịch Y không thể chứa OH- , CO32-. Vậy Y chứa KCl 0,5 mol (BTNT cho Cl) và KHCO3 y mol.
Cho y phản ứng với Ba(OH)2 dư:
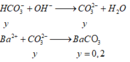
ĐLBKL cho K ta có n(KOH) ban đầu = 0,4x= 0,5 +y = 0,7 => y = 1,75

Đáp án D
Nhỏ từ từ axit vào dung dịch X ⇒ dung dịch Y.
⇒ Y chứa KCl và KHCO3.
Cho Y + dung dịch Ba(OH)2 dư ⇒ có phản ứng.
KHCO3 + Ba(OH)2 → BaCO3 + KOH + H2O.
+ Mà nKHCO3 = nBaCO3 = 0,2 mol.
+ Bảo toàn Cl ⇒ nKCl = nHCl = 0,5 mol.
⇒ Bảo toàn K ⇒ nKOH = nKCl + nKHCO3 = 0,7 mol.
⇒ CM KOH = 0 , 7 0 , 4 = 1,75M

Đáp án D
Nhỏ từ từ axit vào dung dịch X ⇒ dung dịch Y.
⇒ Y chứa KCl và KHCO3.
Cho Y + dung dịch Ba(OH)2 dư ⇒ có phản ứng.
KHCO3 + Ba(OH)2 → BaCO3 + KOH + H2O.
+ Mà nKHCO3 = nBaCO3 = 0,2 mol.
+ Bảo toàn Cl ⇒ nKCl = nHCl = 0,5 mol.
⇒ Bảo toàn K ⇒ nKOH = nKCl + nKHCO3 = 0,7 mol.
⇒ CM KOH = 0 , 7 0 , 4 = 1,75M

Đáp án A
Gọi công thức TB của hai muối cacbonat là: M ¯ C O 3
M ¯ C O 3 → t 0 M O + C O 2 ( 1 )
Chất rắn Y ( M ¯ C O 3 ; M ¯ O )
n C O 2 ( 1 ) = 3 , 36 22 , 4 = 0 , 15 m o l
Y tác dụng với dung dịch HCl dư
M ¯ C O 3 + 2 H C l → t 0 M ¯ C l 2 + C O 2 + H 2 O ( 2 ) M ¯ O + H C l → t 0 M ¯ C l 2 + H 2 O ( 3 ) C O 2 + B a ( O H ) 2 → B a C O 3 + H 2 O ( 4 ) 2 C O 2 + B a ( O H ) 2 → B a ( H C O 3 ) 2 ( 5 ) B a ( H C O 3 ) 2 → t 0 B a C O 3 + C O 2 + H 2 O ( 6 ) n B a C O 3 ( 4 ) = 9 , 85 197 = 0 , 05 m o l n B a C O 3 ( 6 ) = 9 , 85 197 = 0 , 05 m o l
Theo PT (4,5,6): n C O 2 ( 3 ) = 0 , 15 m o l
Theo PT (1,2):
n M ¯ C O 3 = n C O 2 ( 2 ) + n C O 2 ( 1 ) = 0 , 15 + 0 , 15 = 0 , 3 m o l
Muối khan là: M ¯ C l 2
M ¯ C O 3 → M ¯ C l 2 M ¯ + 60 M ¯ + 71
0,3 mol muối cacbonat pư tạo 0,3 mol muối clorua tăng 3,3(g).
Khối lượng muối cacbonat ban đầu là: 38.15-3,3= 34,85(g)
Giá trị của m = 34,85(g)

Đáp án C
Bảo toàn nguyên tố cho cacbon ta có
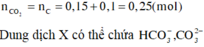
Thứ tự các phản ứng xảy ra khi cho từ từ dung dịch H+ vào dung dịch X là
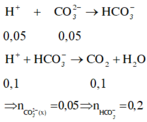
Các phản ứng tạo thành các chất trong dung dịch X
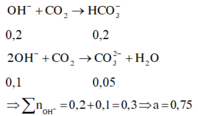
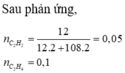
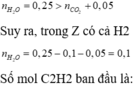


Đáp án A
Ba+ 2H2O → Ba(OH)2+ H2
Na + H2O → NaOH + 1 2 H2
Đặt nBa = x mol; nNa = y mol → mhỗn hợp = 137x + 23y = 17,15 gam
n H 2 = x+ 1 2 y = 3,92/22,4 = 0,175 mol ; n O H - = 2. n H 2 = 0,35 mol
Giải hệ trên ta có: x= 0,1 mol ; y=0,15 mol
Để giải bài này ta nên sử dụng phương trình phân tử :
Sục khí CO2 vào dung dịch Y chứa NaOH, Ba(OH)2 thì xảy ra các PTHH sau:
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O (1)
CO2+ 2NaOH → Na2CO3+ H2O (2)
CO2+ Na2CO3+ H2O→ 2NaHCO3 (3)
CO2+ BaCO3+ H2O → Ba(HCO3)2 (4)
Để lượng kết tủa thu được lớn nhất thì BaCO3 không bị hòa tan
→Lượng CO2 nhỏ nhất khi xảy ra phản ứng (1), còn lượng CO2 lớn nhất khi xảy ra phản ứng (1), (2), (3)
-KHi xảy ra phản ứng (1): n C O 2 = n B a ( O H ) 2 = x = 0,1 mol
-Khi xảy ra cả phản ứng (1,2,3):
n C O 2 = n B a ( O H ) 2 + 1 2 n N a O H + n N a 2 C O 3
= 0,1+0,5 .0,15+ 0,5.0,15 = 0,25 mol
→ 0,1 ≤ n C O 2 ≤ 0,25 mol→2,24 ≤ V C O 2 ≤ 5,6