Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : A
Bảo toàn điện tích : nH+ + 3nAl3+ = nNO3- + 2nSO4 => 3a – b = -0,06
, nOH = nKOH + 2nBa(OH)2 = 0,168 mol ; nBa2+ = 0,012 mol
, mkết tủa = mBaSO4 + mAl(OH)3 => nAl(OH)3 = 0,012 mol < 1/3( nOH – nH+)
=> Có hiện tượng kết tủa tan 1 phần => nAl(OH)3 = 4nAl3+ - (nOH- - nH+)
=> nAl3+ = a = 0,02 => b = 0,12

Đáp án : A
nBa2+ = 0,04 mol ; nOH = 0,32 mol
=> Kết tủa gồm 0,04 mol BaSO4 và Al(OH)3
=> nAl(OH)3 = 0,04 mol
Vì 3nAl(OH)3 < (nOH – nH+) => có sự hòa tan kết tủa
=> nAl(OH)3 = 4nAl3+ - (nOH – nH+)
=> nAl(OH)3 = z = 0,06 mol
Bảo toàn điện tích trong dung dịch X : nH+ + 3nAl3+ = 2nSO4 + nNO3
=> nNO3 = t = 0,2 mol

Chọn A
Bảo toàn điện tích : 3a + 0,15 = b + 0,03.2 => 3a + 0,09= b mol
Z : nOH = 0,252 mol ; nBa2+ = 0,018 mol < nSO4
=> kết tủa gồm Al(OH)3 và BaSO4 => nAl(OH)3 = 0,018 mol
Giả sử có hiện tượng hòa tan kết tủa => nAl(OH)3 = 4nAl3+ - (nOH- - nH+)
=> nAl3+ = a = 0,03 mol => b = 0,18 mol

Đáp án : D
Bảo toàn điện tích : 3a + 0,15 = b + 0,06
nOH = 0,252 mol ; n B a 2 + = 0,018 mol < n S O 4
=> kết tủa gồm 0,018 mol BaSO4 và Al(OH)3
=> n A l O H 3 = 0,018 mol < 1 3 nOH
=> có hiện tượng hòa tan kết tủa
=> n A l O H 3 = 4 n A l 3 + - n O H - n H +
=> n A l 3 + = a = 0,03 mol
=> b = 0,18 mol

Chọn A
nOH- = 0,06x2 = 0,12 > nNH3 = 0,08 Þ OH- dư Þ Trong X có chứa nNH4+ = 0,08
BTĐT => n S O 4 2 - = (0,12 + 0,08 - 0,l)/2 = 0,05 < nBa2+ = 0,06 Þ Có 0,05 mol BaSO4 kết tủa
Þ Trong Z có nBa2+ = 0,06 - 0,05 = 0,01; nK+ = 0,12; nCl- = 0,1; nOH- = 0,12 - 0,08 = 0,04
Vậy m = 0,01x137 + 0,12x39 + 0,1x35,5 + 0,04x17 = 10,28.

Chọn D.
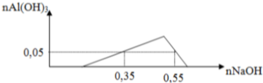
- Tại vị trí n N a O H = 0 , 35 m o l ta có: n H + = n N a O H - 3 n A l ( O H ) 3 = 0 , 2 m o l
- Tại vị trí n N a O H = 0 , 55 m o l ta có: n A l 3 + = n N a O H + n A l ( O H ) 3 - n H + 4 = 0 , 1 m o l
- Xét dung dịch X , áp dụng bảo toàn điện tích ta suy ra: z = 0,2 mol.
- Khi cho 0,27 mol Ba(OH)2 tác dụng với dung dịch X thì kết tủa thu được gồm BaSO4 và Al(OH)3 với
n B a S O 4 = n S O 4 2 - = 0 , 2 m o l n A l ( O H ) 3 = 4 n A l 3 + - n O H - + n H + = 0 , 06 m o l ⇒ m k t u a = 51 , 28 g a m


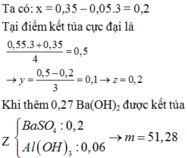

Đáp án B