Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức trung bình của hai muối là: M ¯ 2 CO 3
Cho từ từ hỗn hợp muối cacbonat nên ta có phản ứng:
CO 3 2 - + 2 H + → CO 2 + H 2 O
Sau khi phản ứng với dung dịch axit, thêm Ba(OH)2 dư vào Y thấy xuất hiện kết tủa H+ hết và dư CO 3 2 -
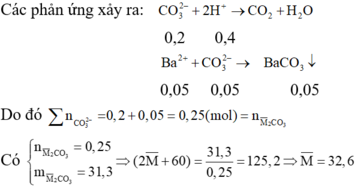
Vậy hai kim loại cần tìm là Na và K
Đáp án B.

Đáp án B
Gọi công thức trung bình của hai muối là: M2CO3.
Sau khi phản ứng với dung dịch axit, thêm Ba(OH)2 dư vào Y thấy xuất hiện kết tủa à H+ hết và dư CO32-
Các phản ứng xảy ra: CO32- + 2H+ → CO2 + H2O
0,2 0,4
CO32-dư + Ba2+ → BaCO3
0,05 0,05 0,05

Đáp án D
Thí nghiệm 1: Khi cho từ từ dung dịch HCl vào muối cacbonat xảy các phương trình theo thứ tự sau:
H+ + CO32- → HCO3- (1)
Sau khi (1) xảy ra nếu H+ dư thì HCO3- + H+ → CO2 + H2O (2)
Thí nghiệm 2: Nhận thấy khi cho dung dịch Ca(OH)2 vào dung dịch thu được của thí nghiệm 1 thấy tạo kết tủa → trong dung dịch còn ion HCO3- : 0,03 mol ( HCO3- + OH- → CO32- )
Bảo toàn nguyên tố C ta có : nmuối = nHCO3- + nCO2 = 0,03 + 0,015 = 0,045 mol
→ Mtb muối =
5
,
25
0
,
045
= 116,67→ 2 muối cacbonat của kim loại kiềm kế tiếp là Na2CO3 và K2CO3
Ta có nH+ = nCO32- + nCO2 = 0,045 + 0,015 = 0,06 mol
Dung dịch HCl có pH = 0 → CMHCl = 1 M → VHCl = 0,06 lít

n CaCO 3 = 0 , 5 ⇒ n CO 3 2 - = 0 , 5
n H 2 SO 4 = 0 , 3 . 0 , 5 = 0 , 15 ⇒ n H + = 0 , 3 ; n SO 4 2 - = 0 , 15
Ta có: n CO 3 2 - > n H + => Chỉ xảy ra phản ứng: H + + CO 3 2 - → HCO 3 - và CO 3 2 - còn dư
Vậy dung dịch Y chứa 6 muối chỉ có thể là
Na2CO3; K2CO3; KHCO3; NaHCO3; Na2SO4; K2SO4
Trong Y chứa các anion: CO 3 2 - ( a mol ) ; HCO 3 - ( b mol ) ; SO 4 2 - ( 0 , 15 mol )
Khi thêm Ba(OH)2 dư vào dung dịch Y ta có các phản ứng:

Ta có a + b = n CO 3 2 - = 0 , 5 ⇒ m = 0 , 5 . 197 + 0 , 15 . 233 = 133 , 45 gam
Đáp án C

Đáp án B
Gọi công thức trung bình của hai muối ACO3 và BCO3 là MCO3
MCO3 → MO + CO2
n C O 2 = 3,36 /22,4 = 0,15 mol → n M C O 3 = 0,15 mol
Hỗn hợp Y gồm MCO3 dư và MO
MCO3 + 2HCl → MCl2 + CO2 + H2O
MO + 2HCl → MCl2 + H2O
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
n C a C O 3 = 15/100 = 0,15 mol
→ n M C O 3 dư = 0,15 mol
n M C O 3 ban đầu = 0,15 + 0,15 = 0,3 mol
Bảo toàn kim loại M có:
n M C O 3 = n M C l 2 = 0,3 (mol)
Bảo toàn khối lượng có:
m M C O 3 = m M C l 2 - 0,3.(71- 60) = 29,2 (gam)

Đáp án B
7,2 gam MCO3 + HCl → CO2 + 0,09 mol Ba(OH)2 → 0,08 mol BaCO3↓
• CO2 + Ba(OH)2 → BaCO3↓ + H2O(*)
BaCO3 + CO2 + H2O → Ba(HCO3)2 (**)
Theo (*) nCO2(*) = 0,09 mol; nBaCO3 (*) = 0,09 mol
Theo (**) nBaCO3 (**) dư = 0,08 mol → nBaCO3 (**) phản ứng = 0,09 - 0,08 = 0,01 mol
→ nCO2 (**) = 0,01 mol → ∑nCO2 = 0,1 mol
• MCO3 + 2HCl → MCl2 + CO2 + H2O
nMCO3 = nCO2 = 0,1 mol → MMCO3 = 7,2 : 0,1 = 72 → MM = 12 → Be và Mg (9 < 20 < 24)


Đáp án B
M2CO3 C → + H C l O2 + dumg dịch X → d u C a ( O H ) 2 0,2 mol CaCO3
Ta có nCO2
Nhận thấy khi cho dung dịch Ca(OH)2 dư vào dung dịch X tạo kết tủa → trong X có chứa HCO3-
Bảo toàn nguyên tố C → nM2CO3 = nCaCO3 + nCO2 = 0,3 mol
Vậy Mtb muối = 35 0 , 3 = 116,67 → Mtb kim loại = 28,33 mà hai kim loại ở chu kì kế tiếp → Na, K. Đáp án B